
【题目】如图所示,p、q、m、n分别为常见的气体单质,p和s均为有色气体,q能在p中燃烧并产生苍白色火焰,v的水溶液呈碱性,t的水溶液呈酸性。回答下列问题:
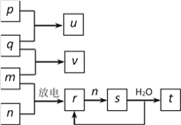
(1)新制p的水溶液中,除H2O、H+、OH-外,还含有____________等粒子(填化学式)
(2)取2份新制p的水溶液,向第一份中滴入紫色石蕊溶液,现象是____________;第二份先滴入FeCl2溶液,后加入KSCN溶液,其现象是_____________,有关反应的离子方程式为_______________、_________________。
(3)反应“v+n→r”的化学方程式是__________,每转移2 mol电子,可生成标准状况下的r气体________L。s溶于水的反应中,氧化剂与还原剂的物质的量之比为________
【答案】 Cl2、HClO、Cl-、ClO- 溶液先变红后褪色 溶液变红 2Fe2++Cl2==2Fe3++2Cl- Fe3++3SCN-==Fe(SCN)3 4NH3+5O2![]() 4NO+6H2O 8.96L 1∶2
4NO+6H2O 8.96L 1∶2
【解析】(1)q能在p中燃烧并产生苍白色火焰,则q为氢气,p为氯气。新制p的水溶液中,发生反应的离子方程式是:Cl2+H2O==H++Cl-+HClO,除H2O、H+、OH-外,溶液中还含有HClO、Cl-、HClO-,及溶解的Cl2等粒子;(2)紫色石蕊溶液加入酸中呈红色,后由于HClO的漂白性而褪色,故实验现象是溶液先变红后褪色;Fe2+会被氧化为Fe3+,加入KSCN溶液后溶液变红,发生了如下反应:2Fe2++Cl2==2Fe3++2Cl-,Fe3++3SCN-==Fe(SCN)3;(3)v的水溶液呈碱性,q为氢气,可知v为氨气,m为氮气,m与n在放电作用下生成r,又与n反应生成有色气体s,可知n为氧气,r为NO,s为NO2,v+n→r的化学方程式是:4NH3+5O2![]() 4NO+6H2O,生成4molNO需要转移电子20mol,则转移2mol电子生成2/5molNO,其体积为8.96L;NO2溶于水的反应为:3NO2+H2O=2HNO3+NO,NO2既为氧化剂又为还原剂,还原产物为NO,氧化产物为HNO3,则发生反应的氧化剂与还原剂的物质的量之比为1:2。
4NO+6H2O,生成4molNO需要转移电子20mol,则转移2mol电子生成2/5molNO,其体积为8.96L;NO2溶于水的反应为:3NO2+H2O=2HNO3+NO,NO2既为氧化剂又为还原剂,还原产物为NO,氧化产物为HNO3,则发生反应的氧化剂与还原剂的物质的量之比为1:2。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下图5个装置都是中学化学中常见的实验装置,某学习小组的同学欲用这些装置进行常见物质的制取并探究其性质(图中a、b、c表示止水夹),请对其进行完善或评价,试回答下列问题:
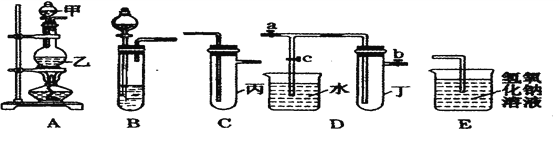
(1)将A、C、E相连后,以浓盐酸和_______(填写名称)为原料制取Cl2,仪器乙的名称是________。写出实验中制备氯气的离子方程式___________________。
(2)利用(1)中装置和药品,在丙中加入适量水,即可制得氯水。将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验实验操作、现象、结论如下:
实验序号 | 实验操作 | 现象 | 结论 |
Ⅰ | 将所得氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
Ⅱ | 向所得氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应至少产生一种酸性强于碳酸的物质 |
实验Ⅰ获得结论是否合理?_________(填“合理”或“不合理”)。若选“不合理”,请说明理由(若选“合理”,则无需填写理由):___________________________________________。
实验Ⅱ获得结论是否合理?_________(填“合理”或“不合理”)。若选“不合理”,请说明理由(若选“合理”,则无需填写理由):______________________________________________。
(3)利用(1)中装置还可设计一个简单的实验比较Cl-和S2-的还原性强弱。则C中预期出现的现象是______________________________________________________________。
(4)将B、D、E装置相连接(打开止水夹a和止水夹b,关闭止水夹c),在B中盛装浓硝酸和铜片(将铜片放在有孔塑料板上),可制得NO2。一段时间后,欲用D装置探究NO2与水的反应,其操作步骤为:先______________________________,再____________________________以使烧杯中的水进入试管丁,观察现象。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇是生活中常接触到的一种有机化合物,请回答下列问题
(1)饭店中常使用固体酒精,你判断它应是(填混合物或纯净物),质量较差的固体酒精在使用时因燃烧不充分,可能产生有毒气体(写化学式);
(2)在焊接铜漆包线的线头时,常先把线头放在火上烧一下以除去漆层,并立即在酒精中蘸一下就可得光亮的铜线,这个过程中乙醇发生(填氧化反应或还原反应);
(3)乙醇和乙酸可以发生酯化反应,请写出化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,某稀溶液中由水电离产生的c(OH﹣)=10﹣10 molL﹣1 . 下列有关该溶液的叙述正确的是( )
A.该溶液一定呈酸性
B.该溶液中c(H+)可能等于10﹣5 molL﹣1
C.该溶液的pH可能为4也可能为10
D.该溶液有可能呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值。下列有关叙述错误的是
A. 28g 由N2 与CO组成的混合气体中所含的原子数为2NA
B. 78g Na2O2 中所含的阴离子数为NA
C. 0.1molSO2 与0.1molO2充分反应后生成的SO2分子数为0.1 NA
D. 0.1molCu溶于足量稀硝酸中,转移的电子数为0.2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有五种短周期主族元素,它们在周期表中的位置如图所示,已知R元素的最高正化合价与最低负化合价的代数和为0。
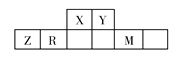
完成下列问题:
(1)Z元素在周期表中的位置是__________________,同周期原子半径最大的元素是____________(填元素符号)。
(2)X的简单氢化物与M的单质,在一定条件下可以发生置换反应,化学方程式为______________,还原产物中含有的化学键类型有____________。
(3)我国发射“神舟”系列飞船的长征火箭,常以X、Y的液态氢化物做燃料。已知X、Y的两种氢化物电子数相等,并且反应时生成两种无毒、无污染的物质。
①写出两种氢化物反应的化学方程式____________________________,反应中氧化剂和还原剂的物质的量之比为____________。
②X的液态氢化物的电子式__________________。
(4)下列说法能证明R、Y非金属性强弱的是____________。
A.R和Y的单质在一定条件下能生成RY2
B.Y单质常温下是气体,R单质是固体
C.Y的氢化物稳定性大于R的氢化物
D.自然界中存在Y单质不存在R单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,其反应原理为:
N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJmol﹣1
一种工业合成氨的简易流程图如下: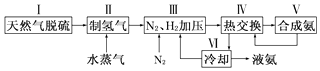
(1)在密闭容器中,使2mol N2和6mol H2混合发生下列反应:N2(g)+3H2(g)2NH3(g)(正反应为放热反应)当反应达到平衡时,N2和H2的浓度比是 . 升高平衡体系的温度(保持体积不变),该反应(填“逆向移动”正向移动”或“不移动”).
(2)氨水、氯水中均存在多种微粒和多个平衡,请写出氯水中存在的一个化学平衡反应的离子方程式 .
(3)步骤Ⅱ中制氢气原理如下:
①CH4(g)+H2O(g)CO(g)+3H2(g)△H=+206.4kJmol﹣1
②CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣41.2kJmol﹣1
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是 .
a.升高温度 b.增大压强 c.加入催化剂 d.降低压强
利用反应②,将CO进一步转化,可提高H2产量.若2mol CO和H2的混合气体(H2的体积分数为80%)与H2O反应,得到2.28mol CO、CO2和H2的混合气体,则CO转化率为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器:①漏斗、②试管、③分液漏斗、④容量瓶、⑤蒸馏烧瓶,常用于物质分离的是 ( )
A. ①③⑤ B. ②③⑤ C. ②④⑤ D. ①②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com