
 控制适合的条件,将反应2Fe3++2I-=2Fe2++I2设计成如图所示的原电池.下列判断不正确的是( )
控制适合的条件,将反应2Fe3++2I-=2Fe2++I2设计成如图所示的原电池.下列判断不正确的是( )

科目:高中化学 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
控制适合的条件,将反应2Fe3++2I- I2+2 Fe2+设计成如图所示的原电池。下列判断不正确的是
I2+2 Fe2+设计成如图所示的原电池。下列判断不正确的是

A 反应从正向开始时,乙中石墨电极上发生氧化反应
 B 电流计读数为零时,反应达到化学平衡状态
B 电流计读数为零时,反应达到化学平衡状态
C 电流计读数为零后,甲乙两烧杯均加等量水稀释,电流计指针不发生偏移
 D
电流计读数为零后,在甲中再溶入FeCl2固体,乙中石墨电极为正极
D
电流计读数为零后,在甲中再溶入FeCl2固体,乙中石墨电极为正极
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江西省高三上学期第四次月考(理综)化学部分 题型:选择题
控制适合的条件,将反应2 Fe 3+ +2I-
 2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是

A. 反应开始时,乙中石墨电极上发生氧化反应

 B. 电流计读数为零后,在甲中溶入FeCl2固体,
B. 电流计读数为零后,在甲中溶入FeCl2固体,
乙中石墨电极为负极
C. 反应开始时,甲中石墨电极上Fe3+被还原
D. 电流计读数为零时,反应达到化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
控制适合的条件,将反应2 Fe 3+ +2I- ![]() 2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是
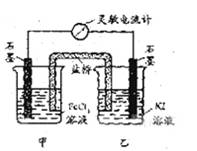
A. 反应开始时,乙中石墨电极上发生氧化反应
B. 电流计读数为零后,在甲中溶入FeCl2固体,
乙中石墨电极为负极
C. 反应开始时,甲中石墨电极上Fe3+被还原
D. 电流计读数为零时,反应达到化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
控制适合的条件,将反应2 Fe 3+ +2I-2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是
A. 反应开始时,乙中石墨电极上发生氧化反应
B. 电流计读数为零后,在甲中溶入FeCl2固体,
乙中石墨电极为负极
C. 反应开始时,甲中石墨电极上Fe3+被还原
D. 电流计读数为零时,反应达到化学平衡状态
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省台州中学高二下学期期中考试化学试卷(带解析) 题型:单选题
控制适合的条件,将反应2Fe3++2I- I2+2 Fe2+设计成如图所示的原电池。下列判断不正确的是
I2+2 Fe2+设计成如图所示的原电池。下列判断不正确的是
 A 反应从正向开始时,乙中石墨电极上发生氧化反应
A 反应从正向开始时,乙中石墨电极上发生氧化反应 B 电流计读数为零时,反应达到化学平衡状态
B 电流计读数为零时,反应达到化学平衡状态 C 电流计读数为零后,甲乙两烧杯均加等量水稀释,电流计指针不发生偏移
C 电流计读数为零后,甲乙两烧杯均加等量水稀释,电流计指针不发生偏移 D 电流计读数为零后,在甲中再溶入FeCl2固体,乙中石墨电极为正极
D 电流计读数为零后,在甲中再溶入FeCl2固体,乙中石墨电极为正极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com