
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
| A、将失去标签的Na2CO3和NaHCO3固体样品配成等物质的量浓度溶液,分别测定pH值,以此鉴别这两种固体 |
| B、用pH试纸分别测定氯水和盐酸的pH值,比较两溶液的酸性强弱 |
| C、取同体积不同浓度的醋酸和盐酸加水稀释相同倍数,测定稀释前后pH值的变化,以此区别这两种酸 |
| D、测定硫酸型酸雨的pH值时,取样后应立即测定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
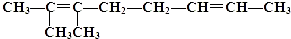 .它与过量的酸性高锰酸钾溶液作用得到下列三种化合物:
.它与过量的酸性高锰酸钾溶液作用得到下列三种化合物: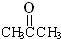 ,
,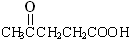 ,CH3COOH.若化合物B与A互为同分异构体,且A、B分别与酸性高锰酸钾溶液反应得到的产物相同,则化合物B的结构简式正确的是( )
,CH3COOH.若化合物B与A互为同分异构体,且A、B分别与酸性高锰酸钾溶液反应得到的产物相同,则化合物B的结构简式正确的是( )| A、CH3CH=C(CH3)-(CH2)2-C(CH3)=CHCH3 |
| B、(CH3)2C=CH-(CH2)2-C(CH3)=CHCH3 |
| C、(CH3)2C=C(CH3)-(CH2)2-CH=CHCH3 |
| D、( CH3)2C=CH-(CH2)2-CH=C(CH3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PH=7的溶液一定显中性 |
| B、PH=6的溶液一定显酸性 |
| C、C(H+)<C(OH-)的溶液一定显碱性 |
| D、C(OH-)=10-6的溶液一定显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将 100g10%的盐酸加热蒸发,得到 50 g溶液,其浓度为20% |
| B、把3mol/L的硫酸与等体积的水混合,所得溶液的浓度大于1.5 mol/L |
| C、把200mL3mol/L的BaCl2溶液跟100mL3mol/L的KCl溶液混合后,溶液中的c(Cl-)仍然是3 mol/L |
| D、已知某温度下KNO3的溶解度是 31.6 g/100 g水,在该温度下将 20 g的KNO3溶于 50 g的水中,所得溶液的质量分数是28.6% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,23g NO2、N2O4的混合气体含有NA个氧原子 |
| B、1L0.1mol?L-1的氨水含有0.1NA个OH- |
| C、常温常压下,22.4LCCl4含有个NACCl4分子 |
| D、1molFe2+与足量的H2O2溶液反应,转移2NA个电子(Fe2+被 H2O2氧化为Fe3+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、蔗糖、硝酸钾和硫酸钡分别属于非电解质、强电解质和弱电解质 |
| C、石炭酸、石油、烧碱分别属于酸、油脂、碱 |
| D、碳酸钠、氢氧化钡、氯化铵、过氧化钠都属于离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com