
| ʵ�鲽�� | ���� | ���� |
| ȡ����NaOH��Һ��Ʒ���Թ��У��ȵμ�������CaCl2��Һ��Ȼ���ٵμӷ�̪��Һ�� | NaOH��Һ���ֱ��� |
���� ��ȫ�����ʣ�����NaOH������ת��Ϊ̼���ƣ����Ȼ��Ʒ�Ӧ����̼��Ƴ�������NaOHӦ���������ܷⱣ�棬�Դ������
��� �⣺��������롿��ͬѧ�IJ���ΪNaOH��Һ���ֱ��ʣ����µIJ���ΪNaOH��Һȫ�����ʣ�
�ʴ�Ϊ��NaOH��Һȫ�����ʣ�
��ʵ��̽���������ֱ��ʣ���ȡ����NaOH��Һ��Ʒ���Թ��У��ȵμ�������CaCl2��Һ��Ȼ���ٵμӷ�̪��Һ���۲쵽������ɫ��������̪��Һ��죻��ȫ�����ʣ�ȡ����NaOH��Һ��Ʒ���Թ��У��ȵμ�������CaCl2��Һ��Ȼ���ٵμӷ�̪��Һ���۲쵽������ɫ��������̪��Һ����ɫ�����ɳ��������ӷ�ӦΪCa2++CO32-=CaCO3����
�ʴ�Ϊ����ɫ��������̪��Һ�����ɫ��������̪��Һ����ɫ��Ca2++CO32-=CaCO3����
��ʵ�鷴˼����1��ѡ����Լ�Ҫ��ֻ�ܹ���̼���Ʒ�Ӧ�������������ܹ�����̼���ƵĴ��ڣ����ܹ��ų�̼���Ƽ��Զ��������Ƶĸ��ţ���˲��ܲ����µļ������ʣ�BaCl2��Һ��Ca��NO3��2��Һ���ܹ���Na2CO3��Ӧ������������û�в����������ʣ���Ca��OH��2��Ba��OH��2��Һ��Na2CO3��Ӧ����CaCO3������OH-����˵μӷ�̪��Һ��ɺ�ɫ������˵����ԭ�е�NaOH�����ã����ܵó����ֱ��ʵĽ��ۣ�
�ʴ��ǣ��ۢܣ�
��2�������������Ƴ����ܹ�ʹָʾ����ɫ�⣬���ܹ�������ͭ���Ȼ����Ȳ�����ɫ����ɫ�IJⶨ���ܹ����Ȼ�立�Ӧ�����̼�����ζ�İ�������˿������������������ƵĴ��ڣ���ѡ������ͭ�����ӷ�ӦΪCu2++2OH-=Cu��OH��2����
�ʴ�Ϊ������ͭ��Һ�����Ȼ�����Һ��NH4Cl��Һ�ȣ���Cu2++2OH-=Cu��OH��2����
����չӦ�á�����ʵ��֤�������������׳�����������еĶ�����̼��Ӧ����̼���ƣ�����Ӧ���ܷⱣ�棬�ʴ��ǣ��ܷⱣ�森
���� ���⿼�����ʵļ���ʵ����ƣ�Ϊ��Ƶ���㣬�������ʵ����ʡ������ķ�Ӧ�����Ӽ��鷽��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע���Լ���ѡ��������Ŀ�ѶȲ���


 �����������ҵ�������������ϵ�д�
�����������ҵ�������������ϵ�д� ѧ���������ν��Ͼ���ѧ������ϵ�д�
ѧ���������ν��Ͼ���ѧ������ϵ�д� Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
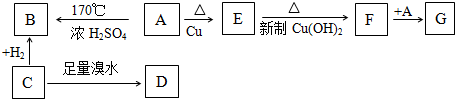
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��C��E�γɻ�����ĵ���ʽ
��C��E�γɻ�����ĵ���ʽ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3�� | B�� | 4�� | C�� | 5�� | D�� | 6�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ�鷽�� |
| 1����ɰֽ��ĥ���þ��������ˮ���ȣ�����Ӧ����Һ�еμӷ�̪ |
| 2��������з�̪��Һ����ˮ��Ӧ |
| 3��þ����2mol/L�����ᷴӦ |
| 4��������2mol/L�����ᷴӦ |
| 5�����Ȼ�����Һ�еμ�����������Һ������ |
| ʵ������ |
| ��A�� |
| ��B����Ӧ��ʮ��ǿ�ң��������� |
| ��C�����ҷ�Ӧ���������� |
| ��D�����ɰ�ɫ��״������Ȼ�������ʧ |
| ��E��������������ڿ�����ȼ�գ���Һ���dz��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ��Һһ������NH4+��I- | |
| B�� | ԭ��Һһ������Ba2+��Fe3+��I- | |
| C�� | ԭ��Һ���ܴ���K+��Fe3+��SO42- | |
| D�� | ��ȡ��Һ�μ��������ᡢBaCl2��Һ������ȷ����Һ���е�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
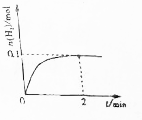 һ���¶��£���2L�ܱ������м���1molNH3��g����������Ӧ2NH3��g��?3H2��g��+N2��g����H=+92kJ/mol
һ���¶��£���2L�ܱ������м���1molNH3��g����������Ӧ2NH3��g��?3H2��g��+N2��g����H=+92kJ/mol�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com