
【题目】部分氧化的铁铜合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:下列说法正确的是( )

A. 滤液A中的阳离子为Fe3+、Fe2+、H+
B. 样品中CuO的质量为4.0 g
C. 样品中Fe元素的质量为2.24 g
D. V=896
【答案】C
【解析】
本题考查的是混合物的计算,根据离子的氧化性强弱明确反应过程是解答的关键,侧重解题方法与分析解决问题能力的考查,注意利用极限法与原子守恒法解答。
硫酸足量,氧化性Fe3+>Cu2+>H+,铁离子优先反应,由于滤液A中不含铜离子,且有气体氢气生成,则滤液A中不含铁离子,滤渣3.2克为金属铜,wuzhi d liang wei 3.2/64=0.05mol,即合金样品中总共含有铜元素0.05mol,滤液A中加入足量氢氧化钠溶液,所得滤液灼烧得到的固体3.2克为氧化铁,其物质的量为3.2/160=0.02mol,铁元素的物质的量为0.04mol,滤液A溶质为过量硫酸和硫酸亚铁,而铁元素物质的量为0.04mol,说明参加反应硫酸物质的量为0.04mol,硫酸含氢离子0.08mol,其中部分氢离子生成氢气,另外的氢离子和合金中的氧结合成水了。A. 由上述分析可知,滤液A中阳离子为Fe2+、H+,故错误;B. 滤液中不含铜离子,滤渣3.2克为金属铜,若全部为氧化铜,氧化铜的质量为80×0.05=4.0克,由于部分铜被氧化成氧化铜,则样品中氧化铜的质量一定小于4.0 g,故错误;C. 合金中铁元素的质量为56×0.04=2.24g,故正确;D.合金中铁元素质量为2.24克,铜元素质量为3.2克,故合金中氧原子的物质的量,它结合氢离子0.04mol,所以硫酸中有0.08-0.04=0.04mol氢离子生成氢气,即生成0.02mol氢气,标况下体积为0.02×22.4=0.448L,故错误。故选C。


科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.100mol/L的NaOH溶液滴定10.00mL浓度均为0.100mol/L的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法不正确的是
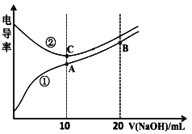
A. 曲线①代表滴定CH3COOH溶液的曲线
B. A、C两点对应溶液均呈中性
C. B点溶液中:c(Na+) > c(OH-) > c(CH3COO-)
D. A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.050mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaCO3与稀盐酸反应生成CO2的量与反应时间的关系如图所示。下列结论不正确的是
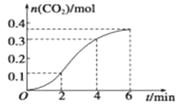
A. 反应在2~4 min内平均反应速率最大
B. 反应开始4 min内温度比浓度对反应速率的影响大
C. 4 min后,反应速率减小的主要原因是c(H+)减小
D. 反应在2~4 min内生成CO2的平均反应速率为v(CO2)=0.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学键的叙述正确的是( )
A.任何物质里都含有化学键
B.离子化合物中可能含有共价键
C.共价化合物分子中可能含有离子键
D.水分子中氢、氧原子间的化学键是非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是

A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e =2CO32-+C
D. 充电时,正极反应为:Na++e=Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]![]() 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。
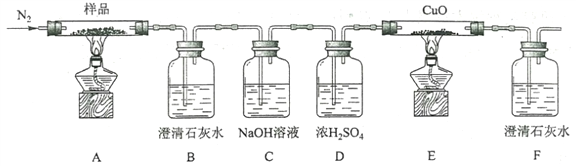
①通入氮气的目的是________________________________________。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________、___________。
③为防止倒吸,停止实验时应进行的操作是_____________________________。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________。
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是___________________________。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学活动小组设计如下图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的气态物质。
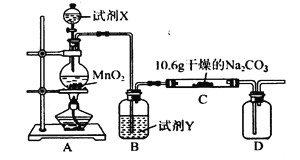
(1)装置A中发生反应的离子方程式为_______________________________________。
(2)装置B中试剂Y应为_________________。
(3)已知在装置C中通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体(含氯氧化物),装置C中只有氯化钠和碳酸氢钠。若C中有0.1 mol Cl2参加反应,可推知C中反应生成的含氯氧化物为______________(写化学式)。
(4)该实验装置中明显存在不足之处,改进的措施为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是化学研究的基础,下列关于各实验装置的叙述正确的是( )

A. 装置③可用于收集H2、CO2、Cl2、NH3等气体
B. 装置②可用于吸收NH3或HCl气体,并防止倒吸
C. 装置①常用于分离互不相溶的液体混合物
D. 装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表中对于相关物质的分类全部正确的一组是( )
编号 | 碱性氧化物 | 酸性氧化物 | 非电解质 | 强电解质 |
A | Na2O | CO2 | NH3 | 醋酸铵 |
B | Na2O2 | SO2 | 乙醇 | NaHCO3 |
C | Al2O3 | SO3 | CO2 | Fe(OH)3 |
D | Fe3O4 | CO | Cl2 | NH4Cl |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com