汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源.冶理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂).它的特点是使CO与NO反应,生成可参与大气循环的无毒气体,并促使烃类充分燃烧及SO2的转化.
(1)写出一氧化碳与一氧化氮反应的化学方程式: .
(2)“催化转化器”的缺点是一定程度上提高了空气的酸度,其原因是 .
A.CO转化为CO2,产生了碳酸酸雾
B.SO2转化为SO3,产生了硫酸酸雾
C.NO转化为NO2,产生了硝酸酸雾
(3)“绿色化学”的最大特点在于从源头上实现污染预防.为控制汽车尾气污染,下列措施符合绿色化学思想的有 (多选扣分).
A.开发氢能源 B.使用电动汽车 C.植树造林 D.戴上呼吸面具.
【答案】
分析:书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须遵守质量守恒定律、依据客观事实.化学反应前后,元素种类不变,原子个数不变.
表示分子或原子团中原子或原子团个数的数字写在元素符号或原子团符号的右下角.
解答:解:(1)一氧化氮和一氧化碳在催化剂的作用下反应生成二氧化碳和氮气.
该反应的化学方程式为:2CO+2NO
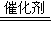
2CO
2+N
2,故答案为:2CO+2NO
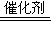
2CO
2+N
2;
(2)A.CO
2不能产生碳酸酸雾,故A错误;
B.SO
2转化为SO
3,产生了硫酸酸雾,故B正确;
C.NO转化为N
2,不产生硝酸酸雾,故C错误;故答案为:B;
(3)A.开发氢能源是从源头上实现污染预防,故A正确;
B.使用电动汽车是从源头上实现污染预防,故B正确;
C.植树造林不是从源头上实现污染预防,故C错误;
D.戴上呼吸面具不是从源头上实现污染预防,故D错误;故答案为:A、B.
点评:本题主要考查化学式的推断和化学方程式的书写,绿色化学的判断,难度不大.

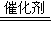 2CO2+N2,故答案为:2CO+2NO
2CO2+N2,故答案为:2CO+2NO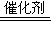 2CO2+N2;
2CO2+N2;

 (1)我国材料科学家师昌绪在合金钢、高温合金及材料强度的研究领域作出杰出贡献,荣获2010年度国家最高科学技术奖.
(1)我国材料科学家师昌绪在合金钢、高温合金及材料强度的研究领域作出杰出贡献,荣获2010年度国家最高科学技术奖.