
反应:4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率
4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率![]() (X)可表示为 ( )
(X)可表示为 ( )
A.![]() (NH3)=0.010mol?L-1?s-1 B.
(NH3)=0.010mol?L-1?s-1 B.![]() (O2)=0.0010mol?L-1?s-1
(O2)=0.0010mol?L-1?s-1
C.![]() (NO)=0.0010mol?L-1?s-1 D.
(NO)=0.0010mol?L-1?s-1 D.![]() (H2O)=0.045mol?L-1?s-1
(H2O)=0.045mol?L-1?s-1
科目:高中化学 来源: 题型:
 (2010?普陀区二模)一定条件下密闭容器中发生反应:4NH3(g)+5O2(g)
(2010?普陀区二模)一定条件下密闭容器中发生反应:4NH3(g)+5O2(g)| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
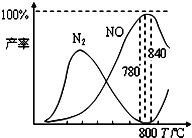 (2012?太原一模)氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生如下①主反应和②副反应:
(2012?太原一模)氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生如下①主反应和②副反应:查看答案和解析>>
科目:高中化学 来源: 题型:
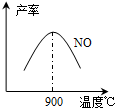 工业合成氨与制备硝酸一般可连续生产,流程如下:
工业合成氨与制备硝酸一般可连续生产,流程如下: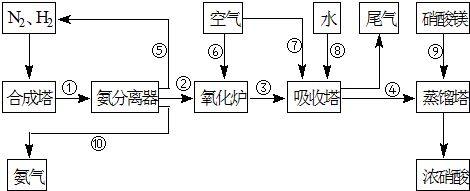
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(NH3)=0.02mol?L-1?s-1 | B、v(O2)=0.01mol?L-1?s-1 | C、v(N2)=0.02mol?L-1?s-1 | D、v(H2O)=0.02mol?L-1?s-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com