
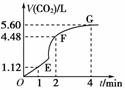
向200 mL 6 mol/L的盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定)。
请回答下列问题:
(1)设OE段的反应速率为v1,EF段的反应速率为v2,FG段的反应速率为v3,则速率从大到小的顺序为____________。(用v1、v2、v3表示)
(2)为了减缓上述反应的速率,欲向该溶液中加入下列物质,你认为可行的是________(填字母)。
A.蒸馏水 B.氯化钾固体
C.氯化钠溶液 D.浓盐酸
E.降低温度 F.减少CaCO3
(3)若反应过程中溶液体积的变化忽略不计,计算FG段用盐酸表示的化学反应速率是多少?(写出计算过程)
科目:高中化学 来源: 题型:
在浓盐酸中H3AsO3与SnCl2的离子方程式为:3SnCl2+12Cl-+6 H++2H3AsO3=== 2As +3SnCl62-+6M,关于该反应的说法中正确的组合是
①氧化剂是H3AsO3 ②还原性:Cl->As ③ 每生成1mol As,反应中转移电子的物质的量为3 mol ④ M为OH- ⑤ SnCl62-是氧化产物
A.①③⑤ B.①②④⑤ C.①②③④ D.只有①③
查看答案和解析>>
科目:高中化学 来源: 题型:
向某溶液中加入含有Fe2+的溶液后,无明显变化。当再滴入几滴新制氯水后,混合溶液变成红色,则下列结论错误的是( )
A.该溶液中一定含有SCN- B.氧化性:Fe3+>Cl2
C.Fe2+与SCN-不能形成红色物质 D.Fe2+被氧化为Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下在密闭容器中能表示可逆反应2SO2+O22SO3一定达到平衡状态的是( )
①消耗2 mol SO2的同时生成2 mol SO3
②SO2、O2与SO3的物质的量之比为2∶1∶2
③反应混合物中SO3的浓度不再改变
A.①② B.②③
C.只有③ D.只有①
查看答案和解析>>
科目:高中化学 来源: 题型:
在O2、H2、Cl2、HCl、CO、CO2等气体中:
(1)无色、无刺激性气味,但有毒的是________。
(2)有色、有刺激性气味的是________。
(3)可用排水法收集的是____________。
(4)在其水溶液中滴入石蕊溶液,先变红,后退色的是_______________________。
(5)常做氧化剂的是________,在高温条件下常做还原剂的是__________。
(6)不可用排水法收集的是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行下列反应:X2(g)+Y2(g)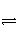
 2Z(g)。已知X2、Y2和Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1和0.2 mol·L-1,当反应在一定条件下达到平衡时,各物质的浓度有可能是( )
2Z(g)。已知X2、Y2和Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1和0.2 mol·L-1,当反应在一定条件下达到平衡时,各物质的浓度有可能是( )
A.Z为0.3 mol·L-1 B.Y2为0.4 mol·L-1
C.X2为0.2 mol·L-1 D.Z为0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
碳酸铵[(NH4)2CO3]在室温下就能自发地分解产生氨气,对其说法正确的是( )
A.碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大
B.碳酸铵分解是因为外界给予了能量
C.碳酸铵分解是吸热反应,根据能量判据不能自发分解
D.碳酸盐都不稳定,都能自发分解
查看答案和解析>>
科目:高中化学 来源: 题型:
对达到平衡状态的可逆反应X+Y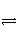
 Z+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图所示,则X、Y、Z、W 4种物质的聚集状态为( )
Z+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图所示,则X、Y、Z、W 4种物质的聚集状态为( )
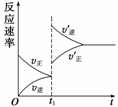
A.Z、W均为气体,X、Y中有一种是气体
B.Z、W中有一种是气体,X、Y皆非气体
C.X、Y、Z、W皆非气体
D.X、Y均为气体,Z、W中有一种为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
巴豆酸的结构简式为CH3—CH===CH—COOH,现有:①氯化氢 ②溴水 ③纯碱溶液 ④2丙醇 ⑤酸化的高锰酸钾溶液。试根据巴豆酸的结构特点判断在一定条件下能与巴豆酸反应的物质有( )
A.②④⑤ B.①③④
C.①②③④ D.①②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com