科学家一直致力于“人工固氮”的新方法研究.最新“人工固氮”的研究报道,在常温、常压、光照条件下,N
2在催化剂表面与水发生下列反应:
2N
2(g)+6H
2O(l)

4NH
3 (g)+3O
2(g)△H=a kJ?mol
-1上述反应NH
3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
| 温度 T/K |
303 |
313 |
323 |
| NH3生成量/(10-6mol) |
4.8 |
5.9 |
6.0 |
(1)此合成反应的a
>
>
0 (填“>”“<”或“=”)
(2)用水稀释0.1mol?L
-1氨水,溶液中随着水量的增加而减小的是
AD
AD
(填字母标号)
A.
B.
C.c(H
+)?c(OH
-) D.
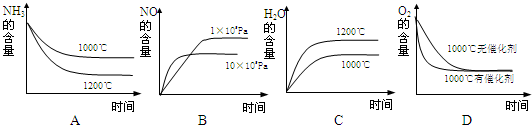
(3)氨可用于工业制硝酸,其主反应为:
4NH
3(g)+5O
2(g)═4NO(g)+6H
2O(g)△H<0
若此反应起始的物质的量相同,则下列关系图正确的是
BD
BD
(填序号)
(4)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 时间/浓度 |
c(NH3) (mol/L) |
c(O2 ) (mol/L) |
c(NO) (mol/L) |
| 起始 |
0.8000 |
1.600 |
0.000 |
| 第2min |
0.6000 |
a |
0.2000 |
| 第4min |
0.3000 |
0.9750 |
0.5000 |
| 第6min |
0.3000 |
0.9750 |
0.5000 |
| 第8min |
0.7000 |
1.475 |
0.1000 |
①反应在第2min到第4min时,O
2 的平均反应速率为
0.1875
0.1875
mol/(L?min)
②反应在第2min到第4min时改变了条件,改变的条件可能是
升高温度或使用催化剂
升高温度或使用催化剂
.
③在第6min到第8min时,改变了反应的条件,该平衡向
左
左
移动(填“左”或“右”).

 4NH3 (g)+3O2(g)△H=a kJ?mol-1
4NH3 (g)+3O2(g)△H=a kJ?mol-1


 中考解读考点精练系列答案
中考解读考点精练系列答案

 。设在容积为2.0 L的密 闭容器中充人0. 60 mol N2(g)和l.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。计算
。设在容积为2.0 L的密 闭容器中充人0. 60 mol N2(g)和l.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。计算  的平衡常数。
的平衡常数。