
【题目】肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H2O):CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4·H2O+NaCl。

实验一:制备NaClO溶液(实验装置如图1所示)
(1)锥形瓶中发生反应的离子方程式是________________________________________________。
实验二:制取水合肼.(实验装置如图2所示)
已知水合肼具有还原性,被氧化生成氮气。
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。
(2)分液漏斗中的溶液是______(填标号).
A.CO(NH2)2溶液 B.NaOH和NaClO混合溶液
选择的理由是____________________________________________________。
实验三:测定馏分中水合肼的质量分数。采用下列步骤:
a.称取馏分5.000g,加入适量NaHCO3固体,加水配成250mL溶液。
b.移取25.00mL溶液于锥形瓶中,加入10mL水,摇匀。
c.用0.2000 mol·L-1的I2溶液滴定,至溶液出现微黄色且半分钟内不消失,滴定过程中,溶液的pH保持在6.5左右,记录消耗碘的标准溶液的体积。
d.进一步操作与数据处理。
(3)水合肼与碘溶液反应的化学方程式为:_______________________;
(4)滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是_______________。
(5)滴定时,碘的标准溶液盛放在___________(填“酸式”或“碱式”)滴定管中;若三次滴定消耗碘的标准溶液的平均体积为18.00mL,则馏分中水合肼(N2H4·H2O)的质量分数为____________________(保留三位有效数字)。
【答案】 Cl2+2OH-=ClO-+Cl-+H2O B 如果次氯酸钠溶液装在烧瓶中,反应生成的水合肼会被次氯酸钠氧化 N2H4H2O +2I2=N2↑+4HI+H2O 生成的HI与NaHCO3反应 酸式 18.0%
【解析】(1)氯气通入到盛有NaOH的锥形瓶中发生反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH﹣=ClO﹣+Cl﹣+H2O;
故答案为:Cl2+2OH﹣=ClO﹣+Cl﹣+H2O;
(2)依据制取水合肼(N2H4H2O)的原理:CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4H2O+NaCl,可知,要将CO(NH2)2溶液与NaOH和NaClO混合溶液加在一起发生反应。根据题中的已知信息,“水合肼具有还原性,被氧化生成氮气。”可知,水合肼能被强氧化性的NaClO氧化成氮气,所以NaOH和NaClO混合溶液一定不能过量。则要将NaOH和NaClO混合溶液滴入CO(NH2)2溶液中,即分液漏斗中装NaOH和NaClO混合溶液。
故答案为:B;如果次氯酸钠溶液装在烧瓶中,反应生成的水合肼会被次氯酸钠氧化;
(3)水合肼与碘溶液反应发生氧化还原反应,生成N2、HI和H2O,反应的化学方程式为:N2H4H2O+2I2=N2↑+4HI+H2O;
故答案为:N2H4H2O+2I2=N2↑+4HI+H2O;
(4)NaHCO3能控制溶液的pH在6.5左右,是因为生成的HI与NaHCO3 反应;
(5)碘单质具有氧化性,应选择酸式滴定管;结合反应定量关系计算水合肼(N2H4H2O)的质量分数,
N2H4H2O+2I2=N2↑+4HI+H2O;
1 2
n 0.2000mol/L×0.018L
n=0.0018mol
250ml溶液中含有的物质的量=0.0018mol×![]() =0.018mol
=0.018mol
水合肼(N2H4H2O)的质量分数=![]()
故答案为:酸式,18.0%


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】实验室制取少量干燥的氨气涉及下列装置中,其中正确的是( )
A.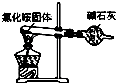
如图是氨气发生装置
B.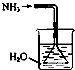
如图是氨气吸收装置
C.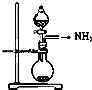
如图是氨气发生装置
D.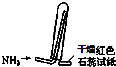
如图是氨气收集、检验装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有丰富的镁资源.某同学设计了从模拟海水中制备MgO的实验方案: 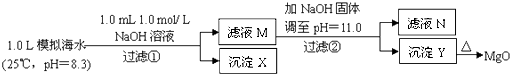
模拟海水中的 | Na+ | Mg2+ | Ca2+ | Cl﹣ | HCO3﹣ |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某种离子的浓度小于1.0×10﹣5 mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变.已知:Ksp(CaCO3)=4.96×10﹣9;Ksp(MgCO3)=6.82×10﹣6;Ksp[Ca(OH)2]=4.68×10﹣6;Ksp[Mg(OH)2]=5.61×10﹣12 . 下列说法正确的是( )
A.沉淀物X为CaCO3
B.滤液M中存在Mg2+ , 不存在Ca2+
C.滤液N中存在Mg2+、Ca2+
D.步骤②中若改为加入4.2gNaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,满足表中图示物质在一定条件下一步转化关系的组合有
序号 | X | Y | Z | W |
|
① | Si | Na2SiO3 | H2SiO3 | SiO2 | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A. ①②③ B. ①③④ C. ②③ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在25 mL 0.1mol/L的NaOH溶液中,逐滴加入0.2 mol/L的CH3COOH溶液,液pH与CH3COOH溶液体积关系如下图所示,下列有关粒子浓度大小关系正确的是
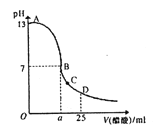
A. a=12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
B. C点时溶液中有: c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C. D点时溶液中有: c(CH3COO-) + c(CH3COOH)=2c (Na+)
D. 曲线上A、B间的任意一点,溶液中都有: c(Na+)>c(CH3COO-) >c(H+) >c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( ) 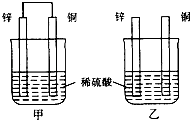
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均减小
D.产生气泡的速度甲比乙快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有两种高聚物A、B,A能溶于苯、四氯化碳等有机溶剂,并加热到一定温度下熔融成粘稠状的液体,B不溶于任何溶剂,加热不会变软或熔融,则下列叙述中不正确的是( )。
A.高聚物A可能具有弹性,而高聚物B没有弹性
B.高聚物A一定是线型高分子材料
C.高聚物A一定是体型高分子材料
D.高聚物B一定是体型高分子材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要化工原料,其产量是一个国家石油化工水平的标志.通过石油裂解可以获得乙烯,再以乙烯为原料还可以合成很多的化工产品.已知乙烯能发生如图转化: 
(1)乙烯的结构简式为 .
(2)反应①的反应类型是 , D中含官能团名称为 .
(3)写出以下反应的化学方程式:①;②;③ .
(4)乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
工艺一: ![]()
工艺二: ![]()
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,在实际生产中,应采用(填“工艺一”或“工艺二”)更环保、更经济.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com