(2009?广东)某工厂生产硼砂过程中产生的固体废料,主要含有MgCO
3、MgSiO
3、CaMg(CO
3)
2、Al
2O
3和Fe
2O
3等,回收其中镁的工艺流程如下:
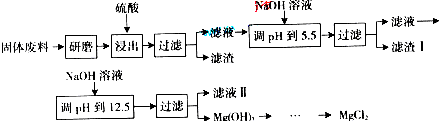
| 沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
| PH |
3.2 |
5.2 |
12.4 |
部分阳离子以氢氧化物形式完全深沉时溶液的pH由见上表,请回答下列问题:
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有
升高温度、搅拌、过滤后再向滤渣中加入硫酸(多次浸取)
升高温度、搅拌、过滤后再向滤渣中加入硫酸(多次浸取)
(要求写出两条).
(2)滤渣I的主要成分有
Fe(OH)3 Al(OH)3
Fe(OH)3 Al(OH)3
.
(3)从滤液Ⅱ中可回收利用的主要物质有
Na2SO4
Na2SO4
.
(4)Mg(ClO
3)
2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
MgCl
2+2NaClO
3═Mg(ClO
3)
2+2NaCl
已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:

①将反应物按化学反应方程式计量数比混合制备Mg(ClO
3)
2.简述可制备Mg(ClO
3)
2的原因:
在某一时NaCl最先达到饱和析出;Mg(ClO3)2的溶解度随温度变化最大;NaCl 的溶解度与其他物质的溶解度有一定的差别.
在某一时NaCl最先达到饱和析出;Mg(ClO3)2的溶解度随温度变化最大;NaCl 的溶解度与其他物质的溶解度有一定的差别.
.
②按①中条件进行制备实验.在冷却降温析出Mg(ClO
3)
2过程中,常伴有NaCl析出,原因是:
降温前溶液中NaCl以达饱和;降低过程中NaCl溶解度会降低,会少量析出
降温前溶液中NaCl以达饱和;降低过程中NaCl溶解度会降低,会少量析出
.除去产品中该杂质的方法是:
重结晶
重结晶
.





 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
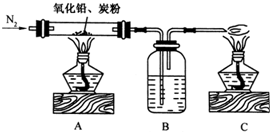 (2009?广东模拟)某课外小组欲通过实验证明方铅矿分解所得白色粉末中含有氧元素,设计以下的实验装置:
(2009?广东模拟)某课外小组欲通过实验证明方铅矿分解所得白色粉末中含有氧元素,设计以下的实验装置:
