
A.氯化铵的电子式: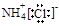 |
B.中子数为21的钾原子: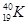 |
C.甲烷分子的球棍模型: |
D.HCO3-水解的离子方程式:HCO3-+H2O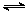 H2CO3+H3O+ H2CO3+H3O+ |
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源:不详 题型:填空题
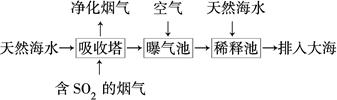
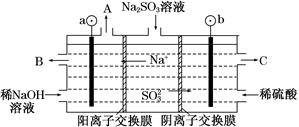
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②③ | C.①③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 H2SO3 + OH– 和 ② (写出离子方程式)
H2SO3 + OH– 和 ② (写出离子方程式)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H2O,则对应的两种物质是 。
H2O,则对应的两种物质是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氧化剂得电子数越多其氧化能力越强 | B.发生化学键断裂的过程不一定发生化学反应 |
| C.常温下所有的吸热反应都不能自发进行 | D.两种难溶物溶解度小的物质其Ksp一定也小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
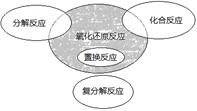
| A.4NH3 +5O2 =4NO+6 H2O |
| B.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| C.2NaHCO3=Na2CO3+H2O+CO2↑ |
| D.Cl2+2NaBr=2NaCl +Br2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com