
下列各组物质中,X是主体物质,Y是少量杂质,Z是为除去杂质所要加入的试剂,其中所加试剂正确的一组是
A | B | C | D | |
X | FeCl2溶液 | FeCl2溶液 | Fe | FeSO4溶液 |
Y | FeCl3 | CuCl2 | Al | Fe2(SO4)3 |
Z | Cl2 | Fe | NaOH溶液 | Cu |
科目:高中化学 来源:2016届甘肃省平凉市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
下列实验中,所采取的分离方法与对应原理都正确的是
选项 | 目的 | 分离方法 | 原理 |
A. | 分离氢氧化铁胶体和氯离子 | 盐析 | 胶体不能透过半透膜,离子能 |
B. | 分离植物油和水的混合物 | 分液 | 二者互不相溶且沸点不同 |
C. | 除去苏打中少量小苏打 | 加热 | 二者的溶解度不同 |
D. | 除去乙醇中的乙酸 | 蒸馏 | 乙醇与乙酸沸点相差较大 |
查看答案和解析>>
科目:高中化学 来源:2016届山东省新高三开学初模拟检测化学试卷(解析版) 题型:选择题
下列说法正确的是
A.光导纤维的主要成分是单质硅
B.新型氢动力汽车的使用可减少雾霾的产生
C.明矾可用于自来水消毒
D.福尔马林可用于食品保鲜
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:
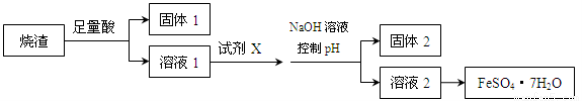
下列说法不正确的是
A.溶解烧渣选用足量硫酸,试剂X选用铁粉
B.固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2
C.从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解
D.若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O
查看答案和解析>>
科目:高中化学 来源:2016届江汉油田海南海政学校高三月考化学试卷(解析版) 题型:填空题
(两个选项符合题意,6分)双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2CO3。关于该物质的说法正确的是( )
A.该物质属于两性氢氧化物
B.该物质是Al(OH)3和Na2CO3的混合物
C.1 mol NaAl(OH)2CO3最多可消耗4 mol H+
D.该药剂不适合于胃溃疡患者服用
18-II(14分)铝是现今人类生产生活中使用广泛性仅次于铁的重要金属。工业上常以“钒土矿”为原料来冶炼金属铝。已知:钒土的主要成分是Al2O3(其中含有Fe2O3、SiO2等杂质)。为了检测某“钒土矿”样中Al2O3的含量,进行了如下实验过程:
①取矿样10.0 g加入过量稀盐酸溶解(假定其他未知成分的杂质都不溶于盐酸,也不和盐酸反应),过滤弃去不溶残渣。
②将滤液稀释并在250 mL容量瓶中定容后,取25.0 mL逐滴滴加2.5 mol·L-1的NaOH溶液,得到如图所示的变化关系。请根据有关数据回答下列问题:
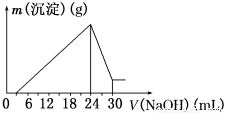
(1)写出滴加NaOH溶液0~3 mL时发生反应的离子方程式:________________。
(2)最后所得不溶于NaOH溶液的沉淀的化学式为______,其物质的量为____________。
(3)该钒土矿样中Al2O3的质量分数为________。
(4)用10.0 t“钒土矿”样提纯所得的Al2O3(提纯过程的损耗忽略不计)进行电解,理论上在 极(填“阴”,“阳”)最多可制得金属铝________t。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省黄石市高三9月调研考试化学试卷(解析版) 题型:填空题
【化学选修3物质结构与性质】(15分)有X、Y、Z、W、P、Q六种前两周期的主族元素,原子序数依次增大,价电子数之和为26,原子半径依Y、Z、W、P、Q、X依次减小。围绕上述元素,回答下列问题:
(1)Q的电子排布图为 ,YQ3中心原子的杂化类型为 ,除X外,其余元素的第一电离能由小到大顺序为 (元素符号回答)。
(2)X2P和ZP2固态时均为分子晶体,但熔点X2P比ZP2高得多,原因是 。
(3)固体A是离子晶体,结构类似于CsCl,组成中含W的质量分数为73.7%,它的所有原子的最外层都符合相应的稀有气体原子的最外层电子结构,该物质适当加热就分解成两种单质气体。该物质的电子式 ,其与水反应的化学方程式为 。
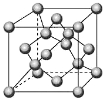
(4)Z单质有三类异形体,其中一种骨架型原子晶体的立方晶胞如图,计算晶体中Z原子的空间利用率为 (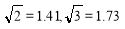 )。
)。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三上学期起点考试化学试卷(解析版) 题型:填空题
【化学—选修3:物质与结构】(15 分)铁和铜都是日常生活中常见的金属,有着广泛的用途。请回答下列问题:
(1)铁的核外电子排布式为 。
(2)配合物Fe(CO)x 常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x 晶体属于______(填晶体类型)。Fe(CO)x 的中心原子价电子数与配体提供电子数之和为18,则x=______。
(3)K3[Fe(CN)6]的配体CN-中碳原子杂化轨道类型为______,C、N、O 三元素的电负性由大到小的顺序为______(用元素符号表示)。
(4)铜晶体铜原子的堆积方式如右图所示。


①铜位于元素周期表的 区。
②每个铜原子周围距离最近的铜原子数目 。
(5)某M 原子的外围电子排布式为3s23p5,铜与M 形成化合物的晶胞如附图所示(黑点代表铜原子)。该晶体中铜原子和M 原子之间的最短距离为a pm,阿伏伽德罗常数为NA,则该晶体的密度为 g/cm3 (只写计算式)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省高一下学期期末考试化学试卷(解析版) 题型:选择题
化学与生活、社会密切相关。下列说法不正确的是
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.提倡人们购物时不用塑料袋,是为了防止白色污染
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com