
����Ŀ��2017��3��21���ǵڶ�ʮ���������ˮ����������ˮ��Դ���������÷�ˮ��ʡˮ��Դ����ǿ��ˮ�Ļ��������ѱ�Խ��Խ���������ע����֪��ij��ɫ��ˮ�п��ܺ���H����NH4+��Fe3����Al3����Mg2����Na����NO3-��CO32-��SO42-�еļ��֣�Ϊ������ɷ֣��ֱ�ȡ��ˮ��Ʒ100mL������������ʵ�飬��������й�ͼ��������ʾ��
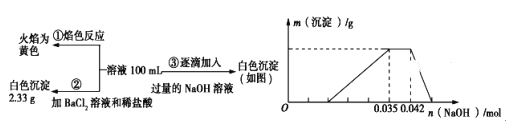
��ش��������⣺
��1����������3��ʵ����Է�����ˮ��һ�������ڵ���������__________��һ�����ڵ���������______________________��
��2��д��ʵ���ͼ���г����ﵽ��������������ٷ����仯�η�����Ӧ�����ӷ�Ӧ����ʽ��_____________________________________________��
��3������ͼ����ԭ��Һ��c(NH4+)��c(Al3��)�ı�ֵΪ___________�����ó��������������_________g��
��4����ͨ��ʵ��ȷ��ԭ��ˮ��c(Na��)=0.14 mol��L-1,���ж�ԭ��ˮ��NO3-�Ƿ���ڣ�__________����������������������������ȷ�������������ڣ�c(NO3-)=____________ mol��L-1�����������ڻ�ȷ����˿ղ��
���𰸡� CO32- Na+��H+��Al3+��NH4+ NH4+ + OH�� = NH3��H2O 1��1 0.546g ���� 0.36 mol��L-1
��������(1)��ɫ��ˮȷ����Fe3+������ʵ���ȷ����Na+������ʵ���ȷ����SO42-������ʵ���ȷ����Al3+��һ������Fe3+��Mg2+����ΪCO32-��Al3+���ܹ��棬������CO32-������Һ�д��ڵ�����Ϊ��Na+��Al3+��NH4+��H+��SO42-����ˮ��һ�������ڵ�������Fe3+��Mg2+��CO32-���ʷ�ˮ��һ�������ڵ���������CO32-��һ�����ڵ���������Na+��Al3+��NH4+��H+��
(2)ʵ���ͼ���г����ﵽ������������μ�NaOH��Һ������Һ���NH4+ ��������NH3��H2O����ʱ�����������ٷ����仯����Ӧ�����ӷ�Ӧ����ʽNH4+ + OH�� = NH3��H2O��
(3)��֪���ᱵ����Ϊ2.33g����n(SO42-)=![]() =0.01mol��
=0.01mol��
����ͼ���֪��Al(OH)3��Ӧ��OH-Ϊ��n(OH-)=0.007mol��
Al(OH)3+OH-=AlO2-+2H2O
n(Al3+) 0.007mol
����n(Al3+)=0.007mol���������ӳ�����Ҫ��������0.021mol��������Һ��H+������������0.014mol�������ӵ����ʵ�����0.014mol��
NH4++OH-=NH3H2O��������������0.007mol������笠����ӵ����ʵ�����0.007mol��ԭ��Һ��c(NH4+)��c(Al3+)�ı�ֵΪ1��1��
����Al(OH)3������Ϊ0.007mol��78g/mol=0.546g��
(4)��Һ�д��ڵ�����Ϊ��Na+��Al3+��NH4+��H+��SO42-����֪���ᱵ����Ϊ2.33g����n(SO42-)=![]() =0.01mol������n(Al3+)=0.007mol��n(H+)=0.014mol��n(NH4+)=0.007mol����Һ�д��ڵ���غ㣬3n(Al3+)+n(H+)+n(NH4+)+n(Na+)=3��0.007mol+0.014mol+0.007mol+0.14 mol��L-1��0.1L=0.056mol��2n(SO42-)=0.02mol����һ������NO3-����n(NO3-)=0.056mol-0.02mol=0.036mol��c(NO3-)=
=0.01mol������n(Al3+)=0.007mol��n(H+)=0.014mol��n(NH4+)=0.007mol����Һ�д��ڵ���غ㣬3n(Al3+)+n(H+)+n(NH4+)+n(Na+)=3��0.007mol+0.014mol+0.007mol+0.14 mol��L-1��0.1L=0.056mol��2n(SO42-)=0.02mol����һ������NO3-����n(NO3-)=0.056mol-0.02mol=0.036mol��c(NO3-)=![]() =0.36mol/L��
=0.36mol/L��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������������ά�ء�������ά�ص����ܼ���ʵ���Һϳɼ�����������ķ�Ӧԭ�����й��������£� ![]() +2C2H5OH
+2C2H5OH ![]()
![]() +2H2O
+2H2O
��Է������� | �ܶ�/��gcm��3�� | �е�/�� | ˮ���ܽ��� | |
����������� | 202 | 1.01 | 245 | ������ˮ |
������ | 146 | 1.36 | 231.8 | �� |
�Ҵ� | 46 | 0.79 | 78.4 | ���� |
�ױ� | 92 | 0.87 | 110.6 | ������ˮ |
ʵ�鲽�����£�
����1����50mLԲ����ƿ�м��뼺����1.8g��0.012mol�����Ҵ�4.4mL��0.076mol�����ױ�5mL��Ũ���ᣨ1mL����װ����ͼ��ʾ��С����Ȼ���40min��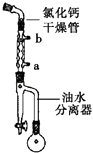
����2����ȴ������װ�ø�Ϊ����װ�ã���ѹ������120�����ҳ������
����3��������2��Һ�嵹�������ƿ�����м�ѹ�������ü����������2.2g��
��1��ͼ������������ȴˮ�����a����b�����ڽ���Ũ�������Ҫ������������ ��
��2������һ��ʱ���ͼ��������������������Ҫ�� ��
��3��ʵ���м���������Ҵ���Ŀ���� ��
��4������2ʵ������ɵı�־�� ��
��5����ʵ��IJ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����Ҫ�Ļ�����Ʒ����ҵ�Ͽ�������ͼ��ʾ��������������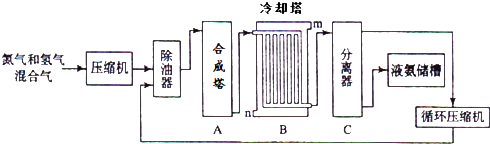
��1��ԭ����֮һ�����Ĺ�ҵ��ȡ������ �� д�������Ĺ�ҵ��;���δ�һ�㣩 ��
��2��д���ϳ����з����ķ�Ӧ�Ļ�ѧ��Ӧ����ʽ ��
����ȴ���жԻ�����������ȴ����ˮ���������m��n����
��3���豸C������ ��
��������еĹ��̶�������ҵ�ϳɰ������� �� ���Խ��ƽ���ƶ�ԭ���ش�
��4����ԭ�����Ʊ������л��� CO�Դ����ж������ã�����ȥԭ�����е� CO����ͨ�����·�Ӧ��ʵ�֣�CO��g��+H2O��g��CO2��g��+H2��g������֪1000Kʱ�÷�Ӧ��ƽ�ⳣ��K=0.627����ҪʹCO��ת������80%������ʼ����c��H2O����c��CO������������ȷ��С�����һλ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ӷ���ʽ��д��ȷ���ǣ� ��
A.NaClO��Һ��FeCl2��Һ��ϣ�6Fe2++3ClO��+3H2O�T2Fe��OH��3��+3Cl��+4Fe3+
B.��ʳ���������е�̼��ƣ�CaCO3+2H+�TCa2++CO2��+H2O
C.FeCl2������Һ���ڿ����б��ʣ�2Fe2++4H++O2�T2Fe3++2H2O
D.���MgCl2ˮ��Һ�����ӷ���ʽ��2Cl��+2H2O ![]() H2��+Cl2��+2OH��
H2��+Cl2��+2OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T�桢2L�ܱ�������ijһ��Ӧ��ͬʱ�̸����ʵ�����ͼ��EΪ���壬����Ϊ���壩���ش��������⣺
��1��д���÷�Ӧ�Ļ�ѧ����ʽ ��
��2����Ӧ��ʼ��3minʱ����D��ʾ��ƽ����Ӧ����Ϊmol/��Lmin����
��3��T��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K= ��
��4����6minʱ�������¶Ȳ��䣬�������������С��ԭ����һ�룬���´ﵽƽ���D���������Ϊ ��
���� | A | B | D | E |
���ʵ���mol | 0.8 | 1.0 | 0.4 | 0.2 |
��5������һ��2L���ܱ�������T�桢ijһʱ��ʱ�������и����ʵ��������ʾ����ʱv������v���棩������ڡ����ڡ���С�ڡ����� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Լ����Ⱥ�˳��,�ɽ����ᡢH2SO4��K2SO4��NaOH��KNO3������ɫ����Һ����������
A. ��ɫʯ����Һ��AgNO3��Һ��ϡ���� B. BaCl2��Һ����ɫ��̪��Һ��AgNO3��Һ
C. ��ɫʯ����Һ��BaCl2��Һ D. ��ɫ��̪��Һ��BaCl2��Һ��AgNO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.������ϵ���¶Ȼ�����ijһ��ֵ�Ũ�Ⱦ������ӷ�Ӧ��ϵ�л������ռ�ٷ���
B.H2+Cl2 ![]() 2HCl��Ӧ�л�ѧ��ֻת��Ϊ����
2HCl��Ӧ�л�ѧ��ֻת��Ϊ����
C.�����������Ҫ���Ͻ��̻�����Ϊ����л��������С���ܱ���������ױ���ȼ��ը
D.����������ȷֽ���һ���ؼ�С�Ĺ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������д������
A. ����Ħ�����ԼΪ22.4L/mol
B. 2 mol N2O��2 mol NO2��ԭ������ͬ
C. ��������O2��O3��������ԭ�Ӹ�����ͬ
D. �����ʵ�����CO��CO2������̼ԭ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ƭ��1 mol��L��1 H2SO4��Ӧ��ȡ����ʱ�����д�ʩ����ʹ�����������ʼӿ����
A. ����������CuSO4��ҺB. ����18 mol��L��1������Һ��Ӧ
C. ������Ƭ����������D. ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com