



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������ҵ���ҹ������д���ʮ����Ҫ��λ�ã���ҵ�ϲ��ø�¯ұ�������ó�����̿���������ۼ���ʯ��ʯ����ԭ�ϣ���֪������ԭ����ԭʱ�����еģ���ԭʱ�¶ȼ�CO��CO2ƽ����������CO����������Ĺ�ϵ��ͼ��
������ҵ���ҹ������д���ʮ����Ҫ��λ�ã���ҵ�ϲ��ø�¯ұ�������ó�����̿���������ۼ���ʯ��ʯ����ԭ�ϣ���֪������ԭ����ԭʱ�����еģ���ԭʱ�¶ȼ�CO��CO2ƽ����������CO����������Ĺ�ϵ��ͼ��| ��Ӧ��� | ��ѧ��Ӧ | ��Ӧ�� |
| �� | Fe2O3��s��+3CO��g��=2Fe��s��+3CO 2��g�� | ��H1=-26.7kJ?mol-1 |
| �� | 3Fe2O3��s��+CO��g��=2Fe3O4��s��+CO2��g�� | ��H2=-50.8kJ?mol-1 |
| �� | Fe3O4��s��+CO��g��=3FeO��s��+CO2 ��g�� | ��H3=-36.5kJ?mol-1 |
| �� | FeO��s��+CO��g��=Fe��s��+CO2��g�� | ��H4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
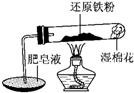 ��֪���¶ȵ���570��ʱ����ԭ������ˮ������Ӧ�IJ�����FeO������570��ʱ������Fe3O4����ʦ��ͼʾʵ��װ�ã�����˻�ԭ������ˮ������Ӧ����ʾʵ�飮
��֪���¶ȵ���570��ʱ����ԭ������ˮ������Ӧ�IJ�����FeO������570��ʱ������Fe3O4����ʦ��ͼʾʵ��װ�ã�����˻�ԭ������ˮ������Ӧ����ʾʵ�飮| ʵ�� ��� |
ʵ����� | ʵ������ |
| �� | ��ȡ������ɫ��ĩ�����Թ��У��������ᣬ�� | ����ɫ��ĩ���ܽ⣬��Һ��dz��ɫ�����������ݲ��� |
| �� | �����Թ��еμӼ���KSCN��Һ���� | ����Һû�г���Ѫ��ɫ |
| A���Թ��ڵĹ���һ���������� |
| B���Թ��ڵĹ���һ��������Fe3O4 |
| C������ȷ���Թ��ڵĹ���һ������FeO |
| D����ͨ�����Թ��ڹ��峹��ԭ��������������С�ķ�����ȷ���Ƿ���Fe3O4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�꽭��ʡ������ѧ����ĩģ�⻯ѧ�Ծ� ���ͣ������
������ҵ���ҹ������д���ʮ����Ҫ��λ�ã���ҵ�ϲ��ø�¯ұ�������ó�����̿���������ۼ���ʯ��ʯ����ԭ�ϡ���֪������ԭ����ԭʱ�����еģ���ԭʱ�¶ȼ�CO��CO2ƽ����������CO����������Ĺ�ϵ����ͼ��

��1������Ԫ�����ڱ���λ�� ���� ��
��2�����¶ȵ���570��ʱ����ԭ��������ɣ����¶ȸ���570��ʱ�����η����Ļ�ԭ��Ӧ�У� ��ѡ����ͼ�е�a��b��c��d��գ�
��3��Ϊ���ٸ�¯ұ��ʱ����CO��β���ŷţ������о�����ȡ���� ��
��a�������������䣬���Ӹ�¯�ĸ߶�
��b�����ڻ�ԭʱ��¯��
��c������ԭ���н�̿�������ı���
��d�������ɵ���ˮ��ʱ�Ƴ�
��4����֪���з�Ӧ��ֵ��
|
��Ӧ��� |
��ѧ��Ӧ |
��Ӧ�� |
|
�� |
Fe2O3(s)��3CO(g)=2Fe(s)��3CO 2(g) |
��H1= -26.7kJ��mol-1 |
|
�� |
3Fe2O3(s)��CO(g)=2Fe3O4(s)��CO2(g) |
��H2= -50.8kJ��mol-1 |
|
�� |
Fe3O4(s)��CO(g)=3FeO(s)��CO2 (g) |
��H3= -36.5kJ��mol-1 |
|
�� |
FeO(s)��CO(g)=Fe(s)��CO2(g) |
��H4 |
��Ӧ�ܡ�H4= kJ��mol-1��
��5��1100��ʱ�� FeO(s)��CO(g)  Fe(s)��CO2(g)��ƽ�ⳣ��K=0.4������һ�ܱ������У�����7.2gFeO��ͬʱͨ��4.48LCO(���ۺ�Ϊ��״��)���������µ�1100�棬��ά���¶Ȳ��䣬��ƽ��ʱ��FeO��ת����Ϊ��
��
Fe(s)��CO2(g)��ƽ�ⳣ��K=0.4������һ�ܱ������У�����7.2gFeO��ͬʱͨ��4.48LCO(���ۺ�Ϊ��״��)���������µ�1100�棬��ά���¶Ȳ��䣬��ƽ��ʱ��FeO��ת����Ϊ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012�꽭��ʡ�߶���ѧ�ڿ�ѧ���Ի�ѧ�Ծ� ���ͣ������
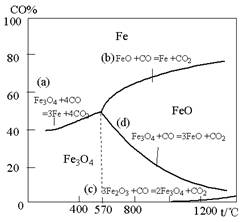
��14�֣�������ҵ���ҹ������д���ʮ����Ҫ��λ�ã���ҵ�ϲ��ø�¯ұ�������ó�����̿���������ۼ���ʯ��ʯ����ԭ�ϡ���֪������ԭ����ԭʱ�����еģ���ԭʱ�¶ȼ�CO��CO2ƽ����������CO����������Ĺ�ϵ����ͼ��
��1������Ԫ�����ڱ���λ�� ���� ��
��2�����¶ȵ���570��ʱ����ԭ��������ɣ����¶ȸ���570��ʱ�����η����Ļ�ԭ��Ӧ�У� ��ѡ����ͼ�е�a��b��c��d��գ�
��3��Ϊ���ٸ�¯ұ��ʱ����CO��β���ŷţ������о�����ȡ���� ��
��a�������������䣬���Ӹ�¯�ĸ߶�
��b�����ڻ�ԭʱ��¯��
��c������ԭ���н�̿�������ı���
��d�������ɵ���ˮ��ʱ�Ƴ�
��4����֪���з�Ӧ��ֵ��
|
��Ӧ��� |
��ѧ��Ӧ |
��Ӧ�� |
|
�� |
Fe2O3(s)��3CO(g)=2Fe(s)��3CO 2(g) |
��H1= -26.7kJ��mol-1 |
|
�� |
3Fe2O3(s)��CO(g)=2Fe3O4(s)��CO2(g) |
��H2= -50.8kJ��mol-1[��Դ:ѧ.��.��] |
|
�� |
Fe3O4(s)��CO(g)=3FeO(s)��CO2 (g)[��Դ:ѧ+��+��] |
��H3= -36.5kJ��mol-1 |
|
�� |
FeO(s)��CO(g)=Fe(s)��CO2(g) |
��H4 |
��Ӧ�ܡ�H4= kJ��mol-1��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com