
无水氯化铝是有机化工常用催化剂,其外观为白色固体,178℃时升华,极易潮解,遇水后会发热并产生白雾。实验室用如下装置制备少量无水氯化铝,其反应原理为:2Al + 6HCl(g) → 2AlCl3 + 3H2。
完成下列填空:

(1)写出B处烧瓶中发生反应的化学方程式:_______________________________________。
(2)C中盛有的试剂为__________。进行实验时应先点燃_____(选填“B”或“D”)处酒精灯。
(3) 用粗短导管连接D、E的目的是_________(选填序号)。
a. 防堵塞 b. 防倒吸 c. 平衡气压 d. 冷凝回流
E瓶的作用是_______________________________________________________。
(4)F中盛有碱石灰,其目的是_________(选填序号)。
a. 吸收HCl b. 吸收Cl2 c. 吸收CO2 d. 吸收H2O
(5)①将D中固体改为市售氯化铝(AlCl3·6H2O)也能进行无水氯化铝的制备,此时通入HCl气体的目的是_____________________________________________。
②若实验条件控制不当,最终得到的物质是碱式氯化铝[化学式为Al2(OH)nCl(6-n)],且质量是原市售氯化铝的40%,则可推算n的值为_______。
(6)有人建议将上述装置A、B中的试剂改为浓盐酸和二氧化锰,其余装置和试剂均不变,也能制备无水AlCl3。事实证明这样做比较危险,请简述理由 _________________________。
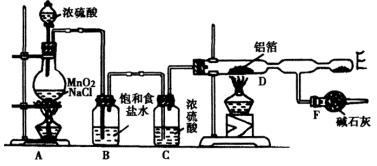
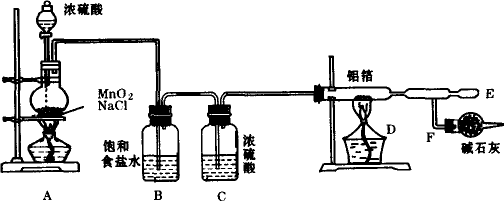
(本题共12分)(1) NaCl + H2SO4(浓) 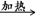 NaHSO4 + HCl↑(1分,写强热亦可,产物为Na2SO4); (2)浓硫酸(1分),B(1分);
NaHSO4 + HCl↑(1分,写强热亦可,产物为Na2SO4); (2)浓硫酸(1分),B(1分);
(3)a(1分);使AlCl3冷凝、收集AlCl3(1分);
(4)ad(2分);
(5)①抑制AlCl3水解(1分);②4(2分);
(6)制得的Cl2中混有HCl,与Al反应生成H2,H2与Cl2混合加热时会发生爆炸(共2分,回答含有HCl得1分,氢氯混合爆炸1分)
【解析】
试题分析:(1)根据氯化铝的制备原理可知,B装置是制备氯化氢的,所以该处反应的化学方程式为NaCl + H2SO4(浓) 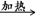 NaHSO4 + HCl↑。
NaHSO4 + HCl↑。
(2)由于氯化铝极易潮解,遇水后会发热并产生白雾,而生成的氯化氢中一定含有水蒸气,所以C装置的作用是干燥氯化氢,因此C中盛放的试剂是浓硫酸。
(3)由于氯化铝178℃时升华,熔点低,其蒸汽易凝结为固体,所以用粗短导管连接D、E的目的是防止凝结生成的氯化铝固体堵塞导管,答案选a;同理可知E瓶的作用是使AlCl3冷凝、收集AlCl3。
(4)反应中氯化氢是过量的,氯化氢是酸性气体,因此碱石灰的作用是吸收氯化氢。又因为AlCl3极易潮解,遇水后会发热并产生白雾,而空气中含有水蒸气,所以碱石灰的另一个作用是吸收空气中的水蒸气,答案选ad。
(5)①氯化铝是强酸弱碱盐,Al3+水解生成氢氧化铝和氯化氢,且水解是吸热的,加热促进水解得不到氯化铝,所以通入氯化氢的目的是抑制AlCl3水解。
②最终得到的物质是碱式氯化铝[化学式为Al2(OH)nCl(6-n)],且质量是原市售氯化铝的40%,则根据铝原子守恒可知2×241.5×40%=267-18.5n,解得n=4。
(6)由于浓盐酸易挥发,所以制得的Cl2中混有HCl,而氯化氢与Al反应生成H2,H2与Cl2混合加热时会发生爆炸,因此该方法比较危险。
考点:考查氯化氢、氯化铝制备;气体的除杂、尾气处理;实验方案设计与评价等


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:高中化学习题 题型:022
无水氯化铝是白色晶体,易吸收水蒸气,在178℃升华.装有无水氯化铝的试剂瓶久置在空气中,会吸湿发白雾,甚至炸裂.氯化铝常用于石油化工和有机合成的催化剂.工业上用铝与氯气合成它,或用无水氯化氢与熔态铝反应制得.有某化学小组用图5-19装置制取少量的无水氯化铝.
试回答:
(1)开始实验时,不能先点燃A装置的酒精灯,后打开分液漏斗的活塞,将适量浓![]() 注入烧瓶里,其理由是________.
注入烧瓶里,其理由是________.
(2)A中的化学反应的反应式为________.
(3)在何处(用仪器编号)得到无水氯化铝________.其理由是________.
(4)由A导出的气体,若不经过B、C装置而直接进入D中,对实验的不良影响是________.
(5)F的作用是________.
(6)用氯化铝水溶液蒸发灼热是否可制无水氧化铝,理由是________.
查看答案和解析>>
科目:高中化学 来源:非常讲解·教材全解全析 高中化学 必修1 (山东版) 山东版 题型:058
无水氯化铝是白色晶体,易吸收水分,在178℃升华.装有无水氯化铝的试剂瓶久置潮湿空气中,会自动爆炸并产生大量白雾.氯化铝常作为有机合成和石油化工的催化剂,并用于处理润滑油等.工业上由金属铝和氯气作用或由无水氯化氢气体与熔融金属铝作用而制得.
某课外兴趣小组在实验室里,通过下图装置制取少量纯净的无水氯化铝.
(1)开始实验时,不能先点燃A装置的酒精灯,后打开分液漏斗的活塞,将适量浓硫酸注入烧瓶里,其理由是________.
(2)A装置中发生反应的化学方程式为________.
(3)在E处可收集到纯净的氯化铝,其原因是________.
(4)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生不良的后果是________.
(5)F装置所起的作用有________.
(6)无水氯化铝在潮湿空气中会产生大量白雾,有关反应的化学方程式为________.
查看答案和解析>>
科目:高中化学 来源:上海市虹口区2013年高考一模化学试题 题型:058
无水氯化铝是有机化工常用催化剂,其外观为白色固体,178℃时升华,极易潮解,遇水后会发热并产生白雾.
实验室用如下装置制备少量无水氯化铝,其反应原理为∶2Al+6HCl(g)→2AlCl3+3H2.完成下列填空∶
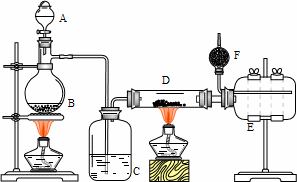
1.写出B处烧瓶中发生反应的化学方程式∶________.
2.C中盛有的试剂为________.进行实验时应先点燃________(选填“B”或“D”)处酒精灯.
3.用粗短导管连接D、E的目的是________(选填序号).
a.防堵塞
b.防倒吸
c.平衡气压
d.冷凝回流
E瓶的作用是________.
4.F中盛有碱石灰,其目的是________(选填序号).
a.吸收HCl
b.吸收Cl2
c.吸收CO2
d.吸收H2O
5.(1)将D中固体改为市售氯化铝(AlCl3·6H2O)也能进行无水氯化铝的制备,此时通入HCl气体的目的是________.
(2)若实验条件控制不当,最终得到的物质是碱式氯化铝[化学式为Al2(OH)nCl(6-n)],且质量是原市售氯化铝的40%,则可推算n的值为________.
6.有人建议将上述装置A、B中的试剂改为浓盐酸和二氧化锰,其余装置和试剂均不变,也能制备无水AlCl3.事实证明这样做比较危险,请简述理由________.
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省邯郸市高三第一次模拟考试理综化学试卷(解析版) 题型:实验题
无水氯化铝是有机化工常用催化剂,其外观为白色固体,178℃时升华,极易潮解,遇水后会发热并产生白雾。实验室用如下装置制备少量无水氯化铝,其反应原理为: 2Al+ 6HCl(g) → 2A1Cl3 + 3H2。

完成下列填空:
(1)写出烧瓶中(B处)发生反应的化学方程式:_____________
(2)C中盛有的试剂为_____。进行实验时应先点燃_____(选填“B”或“D”)处酒精灯。
(3)用粗短导管连接D、E的目的是_______ (选填序号)。
a.防堵塞 b.防倒吸 c.平衡气压 d.冷凝回流
E瓶的作用是_______。
(4)F中盛有碱石灰,其目的是_______(选填序号)。
a.吸收HCl b.吸收Cl2 c.吸收CO2 d.吸收H2O
(5)将D中固体改为市售氯化铝(AlCl3·6H2O)也能进行无水氯化铝的制备,此时通入HCl气体的目的是_______。若实验条件控制不当,最终得到的物质是碱式氯化铝[化学式为Al2(OH)nCl(6-n)],且质量是原市售氯化铝的40%,则可推算n的值为_______。
(6)有人建议将上述装置A、B中的试剂改为浓盐酸和二氧化锰,其余装置和试剂均不变, 也能制备无水AlCl3。事实证明这样做比较危险,请简述理由_______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com