

| A、试剂1可以选用石灰乳 |
| B、从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2═2Cl-+Br2 |
| C、工业上,电解熔融MgO冶炼金属镁可减小能耗 |
| D、可用BaCl2溶液除去粗盐中的SO42- |


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:
| A、2.4 g金属镁变成镁离子时失去的电子数目为6.02×1022 |
| B、2 g氢气所含分子数目为2×6.02×1023 |
| C、在25℃,1.01×105Pa时,11.2 L氧气所含的氧原子数目为6.02×1023 |
| D、标准状况下,以任意比混合的氢气和氧气混合物2.24 L,所含的分子数为6.02×1022 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+、Ba2+、Cl-、SO42- |
| B、Na+、Ba2+、Cl-、NO3- |
| C、Mg2+、K+、Cl-、NO3- |
| D、Na+、K+、NO3-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol/L乙酸溶液的pH约为3 |
| B、乙酸能与水以任何比例互溶 |
| C、10mL1mol/L乙酸恰好与10mL1mol/LNaOH溶液完全反应 |
| D、同温同浓度的乙酸溶液的导电性比硫酸溶液的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 共价键类型 | C-C | C=C | C-H |
| 键能kJ/mol | 332 | 611 | 414 |
| A、C3H8、C2H4、CH4互为同系物 |
| B、C-C比C=C更活泼 |
| C、若1 mol C3H8完全反应,能够吸收53 kJ的热量 |
| D、可用酸性高锰酸钾除去混合气体中的C2H4,得到纯净的CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下pH为5的盐酸溶液稀释1000倍后,pH等于8 |
| B、NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C、在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中阴离子只有CO32-和OH- |
| D、常温下,pH=7的CH3COOH与CH3COONa混合溶液中,c(Na+)=c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
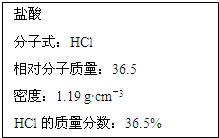 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
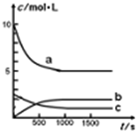 一定温度下,在体积为1L的恒容密闭容器中充入10mol NO2和2.5molO2发生反应:4NO2(g)+O2(g)?2N2O5(g)△H<0.反应混合物中NO2和物质的量浓度随时间的变化如表所示:
一定温度下,在体积为1L的恒容密闭容器中充入10mol NO2和2.5molO2发生反应:4NO2(g)+O2(g)?2N2O5(g)△H<0.反应混合物中NO2和物质的量浓度随时间的变化如表所示:| t/s | 0 | 500 | 1000 | 1500 |
| c(NO2)/mol?L-1 | 10 | 7 | 5 | 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com