
| A.在相同条件下,焓变小于0而熵变大于0的反应肯定能自发进行 |
| B.升高温度会加快化学反应速率,其原因是增加了活化分子的百分数 |
| C.沉淀转换的实质就是沉淀溶解平衡的移动,平衡一般向生成更难溶物质的方向移动 |
| D.PH为10的氨水,由水电离出的氢氧根离子浓度为10-4 mol/L |
科目:高中化学 来源:不详 题型:单选题
| A.任何温度下都是非自发变化 |
| B.高温下是自发进行 |
| C.低温下是非自发变化,高温下是自发变化 |
| D.低温下是自发进行 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.ΔH<0,ΔS>0的反应肯定是自发的 | B.ΔH<0,ΔS<0的反应肯定是自发的 |
| C.ΔH>0,ΔS>0的反应肯定是自发的 | D.ΔH>0,ΔS<0的反应肯定是自发的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.10min时v正=v逆 |
| B.5min时该反应速率v(CH3OH)=0.088mol·L-1·min-1 |
| C.该温度下此反应的平衡常数k=400 |
| D.平衡后其它条件不变,升温,c(CH3OH)=0.06mol/L,该反应△H<0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.N2(g) + 2O2(g) = 2NO2(g) △H =" +" 67.7 kJ/mol |
| B.CaCO3(s) =CaO(s) +CO2(g) △H =" +" 1921.8 kJ/mol |
| C.C6H12O6 ( s ) + 6O2 ( g ) = 6CO2 (g) + 6H2O ( l )△H =" -2804" kJ/mol |
| D.2CO(g)+O2 (g)=2CO2(g)△H= -566 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯化钠溶于水中 | B.NH3(g)和HCl(g)反应生成NH4Cl |
| C.干冰的升华 | D.CaCO3(S)分解为CaO(S)和CO2(g) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
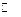 A(g) + 3B(g),(正反应吸热);下列说法正确的是( )
A(g) + 3B(g),(正反应吸热);下列说法正确的是( )| A.升高温度,正反应速率减小,逆反应速率增大, |
| B.降低压强,反应速率减慢,平衡逆向移动 |
| C.达平衡后,升温或加压都有利于平衡正向移动 |
D.达平衡后保持体 积不变,增加C的物质的量,则C的转化率降低 积不变,增加C的物质的量,则C的转化率降低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是| A.达到化学平衡时,5υ正(O2)= 4υ逆(NO) |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态 |
| C.若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| D.催化剂降低反应活化能,增大单位体积内活化分子百分数,从而增大反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com