
| A.+172.51kJ/mol | B.-283.01kJ/mol |
| C.+283.01kJ/mol | D.+504.00kJ/mol |
科目:高中化学 来源:不详 题型:单选题
| A.反应焓变是决定反应能否自发进行的唯一因素 |
| B.固体溶解过程与焓变有关 |
| C.温度、压强一定时,熵增加的反应一定自发进行的反应 |
| D.自发反应在恰当的条件下才能自发 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO3O2 | B.SO2SO3 | C.SO2O2SO3 | D.SO2O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
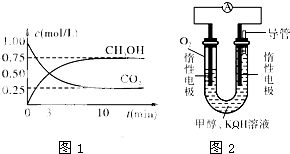
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
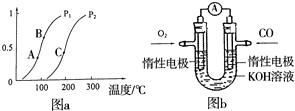
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.天然气、石油、流水、风力、氢气为一级能源 |
| B.无论是风力发电还是火力发电,都是将化学能转化为电能 |
| C.PM 2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 |
| D.发展低碳经济、循环经济,推广利用太阳能、风能的城市照明系统 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 位时间内生成n mol A,同时生成3n mol B
位时间内生成n mol A,同时生成3n mol B 数之比为1:3:2
数之比为1:3:2查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com