
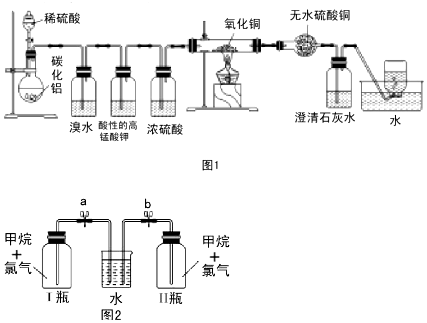
分析 (1)碳化铝(Al4C3)与水反应生成氢氧化铝和甲烷,碳化铝与硫酸反应生成硫酸铝和甲烷;
(2)甲烷与氧化铜反应,碳元素化合价升高,铜元素化合价降低结合甲烷与氧化铜物质的量之比2:7书写;
(3)根据实验甲的实验目的和甲烷的性质进行解答,若集气瓶中收集到的气体属于有毒气体,则不能排放到空气中,反之能;
(4)A.若甲烷能与强氧化剂反应,酸性高锰酸钾溶液褪色;
B.硬质试管里黑色粉末变红色,可能为铜,氧化铜发生了还原反应;
C.氧化铜与甲烷反应生成水和二氧化碳、一氧化碳,硬质试管里黑色粉末也能变红色;
D.甲烷能与卤素单质发生取代反应;
(5)甲烷和氯气在光照条件下发生反应,生成有机物有CH3Cl、CH2Cl2、CHCl3、CCl4,还有无机物氯化氢,根据它们的性质解答.
解答 解:(1)碳化铝(Al4C3)与水反应生成氢氧化铝和甲烷,碳化铝与硫酸反应可理解为碳化铝(Al4C3)与水反应,产物再和硫酸反应,所以产物为硫酸铝和甲烷,反应方程式为:Al4C3+6H2SO4=2Al2(SO4)3+3CH4↑,
故答案为:Al4C3+6H2SO4=2Al2(SO4)3+3CH4↑;
(2)甲烷中碳元素化合价为-4价,甲烷与氧化铜反应,碳元素化合价升高,甲烷与氧化铜物质的量之比2:7,先根据氢守恒确定水前系数,再根据碳、氧守恒得硬质试管里可能发生的化学方程式为:2CH4+7CuO$\frac{\underline{\;\;△\;\;}}{\;}$7Cu+CO+CO2+4H2O,
故答案为:2CH4+7CuO$\frac{\underline{\;\;△\;\;}}{\;}$7Cu+CO+CO2+4H2O;
(3)碳化铝与硫酸反应生成硫酸铝和甲烷,甲方案探究甲烷与氧化剂反应,盛放浓硫酸的装置放置在氧化剂氧化铜之前,所以实验甲中浓硫酸的作用是干燥CH4,甲烷和氧化铜反应,碳元素化合价升高,生成碳的氧化物,产物中可能有一氧化碳生成,所以集气瓶中收集到的气体不能直接排放到空气中,
故答案为:干燥甲烷;不能;
(4)A.甲烷不能与强氧化剂反应,若能反应,则酸性高锰酸钾溶液在甲烷的作用下会褪色,现不褪色,结论是通常条件下,甲烷不能与强氧化剂反应,故A正确;
B.硬质试管里黑色粉末变红色,可能为铜,即黑色的氧化铜被还原为铜单质,氧化铜中铜元素化合价降低,表现氧化性,发生还原反应,故B错误;
C.氧化铜与甲烷反应生成水和二氧化碳、一氧化碳,硬质试管里黑色粉末也能变红色,故C错误;
D.甲烷不能与溴水反应,但甲烷能与卤素单质发生取代反应,故D错误;
故选A;
(5)乙方案中烧杯里放入足量的水,甲烷和氯气在光照条件下发生取代反应,CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl,CH3Cl+Cl2$\stackrel{光照}{→}$CH2Cl2+HCl,CH2Cl2+Cl2$\stackrel{光照}{→}$CHCl3+HCl,CHCl3+Cl2$\stackrel{光照}{→}$CCl4+HCl,生成物中CH3Cl(气体)、CH2Cl2(油状液体)、CHCl3(油状液体)、CCl4(油状液体)、HCl(极易溶于水),打开弹簧夹a、b,一段时间后,观察到有水倒吸到I瓶中,但CH3Cl(气体)难溶于水,所以水并不能充满I瓶,氯气为黄绿色气体、反应后I瓶中气体颜色变浅,HCl(极易溶于水),I瓶中出现白雾,CH2Cl2(油状液体)、CHCl3(油状液体)、CCl4(油状液体)、I瓶瓶内壁出现油状物质,Ⅱ瓶中无现象,II瓶中与I瓶现象不相同,所以ABC符合.
故答案为:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl;ABC.
点评 本题是关于甲烷的还原性的实验探究,考查了元素守恒定律的运用及实验的步骤、物质的性质等,掌握实验室制取氯气的反应原理,明确甲烷的取代反应原理、反应条件是解答关键,试题培养了学生灵活应用所学知识的能力,题目难度中等.


科目:高中化学 来源: 题型:解答题
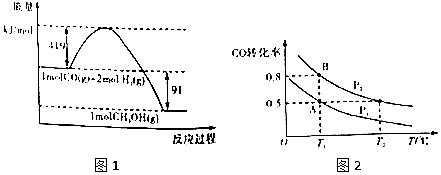
| 化学键 | H-H | H-O | O=O |
| 键能kj/mol | 436 | x | 496 |
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1molCO、2molH2 | 1molCH3OH | 1molCH3OH |
| 平衡时容器体积 | V(甲) | V(乙) | V(丙) |
| 反应的平衡常数K | K(甲) | K(乙) | K(丙) |
| 平衡时CH3OH的浓度/mol•L-1 | C(甲) | C(乙) | C(丙) |
| 平衡时CH3OH的反应速率/mol•L-1•min-1 | v(甲) | v(乙) | v(丙) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg(OH)2+2HCl═MgCl2+2H2O | B. | 2NaOH+H2SO4═Na2SO4+2H2O | ||
| C. | Ba(OH)2+H2SO4═BaSO4↓+2H2O | D. | CH3COOH+NaOH═CH3COONa+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
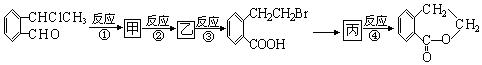
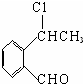 +O2$\stackrel{催化剂}{→}$2
+O2$\stackrel{催化剂}{→}$2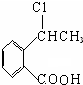 ,氧化反应.
,氧化反应. +NaOH$→_{△}^{CH_{3}CH_{2}OH}$
+NaOH$→_{△}^{CH_{3}CH_{2}OH}$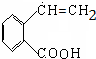 +NaCl+H2O,消去反应.
+NaCl+H2O,消去反应. →丙实际需要两步才能完成,写出第一步反应的化学方程式
→丙实际需要两步才能完成,写出第一步反应的化学方程式 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$ +NaBr+H2O,第二步所用试剂及目的是试剂是盐酸,目的是将钠盐酸化生成对应的酸.
+NaBr+H2O,第二步所用试剂及目的是试剂是盐酸,目的是将钠盐酸化生成对应的酸.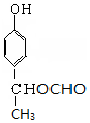 和
和 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯(CH2=CHCH3)易发生加成反应,一定条件下也可能发生取代反应 | |
| B. | 若有机物甲和乙是同分异构体,则甲和乙的化学性质相似 | |
| C. | 某有机物燃烧只生成物质的量之比为l:2 的CO2和H2O,说明其最简式为CH4 | |
| D. | 分子式分别为C2H6O、C3H8O的有机物一定互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在该反应条件下,Mg的还原性强于C的还原性 | |
| B. | Mg、MgO中镁元素微粒的半径:r(Mg2+)<r(Mg) | |
| C. | 元素C 在自然界中既有游离态又有化合态 | |
| D. | 该反应中化学能全部转化为热能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中电能转化为化学能 | |
| B. | 反应低温可以自发转化 | |
| C. | 上述反应若使用催化剂,能改变反应的△H | |
| D. | 反应CH4(g)=C(s)+2H2(g)的△H=74.8kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | lmol Cl2与足量的铁充分反应,.转移的电子数为2NA | |
| B. | 标准状况下,11.2L水所含分子数为0.5NA | |
| C. | 常温常压下,22.4L氖气含有NA个氖原子 | |
| D. | 124g Na2O溶于水后所得溶液中含有O2-离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫单质有氧化性 | B. | 二氧化硫具有还原性 | ||
| C. | 硫酸可以被氧化 | D. | 硫化氢(H2S)可以被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com