
在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是
A.两种气体的压强相等 B.O2比O3的质量小
C.两种气体的分子数目相等 D.两种气体的氧原子数目相等
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
实验室制取硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混合液,加入反应器。
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀。
③在50℃~60℃下发生反应,直到反应结束。
④除去混合酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤。
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏得到纯硝基苯。
填写下列空白:
(1)配制一定比例的浓硫酸和浓硝酸混合酸时,操作注意事项是
________________________________________________________________________。
(2)步骤③中,为了使反应在50℃~60℃下进行,常用的方法是
________________________________________________________________________。
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是____________________________。
(4)步骤④中粗产品用5%NaOH溶液洗涤的目的是_______________________。
(5)纯硝基苯是无色,密度比水________(填“小”或“大”),具有________气味的油状液体。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关合成氨工业的说法中,正确的是 ( )。
A.从合成塔出来的混合气体中,氨气占15%,所以生产氨的工厂的效率都
很低
B.由于氨易液化,N2和H2在实际生产中循环使用,所以总体来说,氨的产
率很高
C.合成氨工业的反应温度控制在500 ℃,目的是使化学平衡向正反应方向
移动
D.我国合成氨厂采用的压强是10~30 MPa,因为该压强下铁触媒的活性最
大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验原理或操作正确的是
A. SO2气体的还原性较强,不能使其通过浓硫酸干燥
 B. 滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定
B. 滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定
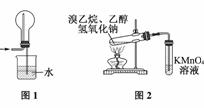
C. 用图1装置吸收多余的HCl气体
D. 用图2装置检验溴乙烷发生消去反应生成乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
恒温(1100℃)恒容密闭容器中发生反应:
Na2SO4(s)+4H2(g) Na2S(s)+4H2O(g)。下列说法正确的是
Na2S(s)+4H2O(g)。下列说法正确的是
A. 该反应的平衡常数表达式K=c(H2O)/c(H2)
B. 若容器内气体的密度或压强保持不变,均说明该反应已达到平衡状态
C. 若Na2SO4足量,改变起始充入H2的浓度,达平衡时H2的转化率不变
D. 若初始时投入2.84gNa2SO4与一定量H2反应达平衡时容器内固体共有2.264g,则Na2SO4的转化率为45%
查看答案和解析>>
科目:高中化学 来源: 题型:
已知气体的摩尔质量越小,扩散速度越快。右下图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于甲、乙的判断正确的是( )
A.甲是浓氨水,乙是浓硫酸 B.甲是浓盐酸,乙是浓氨水
C.甲是浓氨水,乙是浓盐酸 D.甲是浓硝酸,乙是浓氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两烧杯中各盛有100 mL 3 mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则加入铝粉的质量为( )
A.5.4g B.3.6g C.2.7g D.1.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价绝对值相等,Z的核电荷数是Y的2倍,W最外层电子数是最内层电子数的3倍.下列说法正确的是
A.微粒半径:Z2+>W2->R-
B.对应氢化物的稳定性:W>R
C.W与X、W与Z形成的化学物晶体类型相同
D.Y的最高价氧化物对应的水化物是弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中加入A、B、C三种气体,在温度为T K和(T+10)K时,测得各物质的浓度如下表。据此下列结论正确的是( )
| 温度 | T K | (T+10) K | |||
| 测定时刻/s | t1 | t2 | t3 | t4 | t5 |
| c(A)/mol·L-1 | 6 | 3 | 2 | 2 | 2.2 |
| c(B)/mol·L-1 | 5 | 3.5 | 3 | 3 | 3.1 |
| c(C)/mol·L-1 | 1 | 2.5 | 3 | 3 | 2.9 |
A.在t3时刻反应已经停止
B.升高温度,该反应的化学平衡常数将增大
C.在t3时刻,若增大压强,则A的转化率将减小
D.在t2~t3内A的平均反应速率为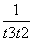 mol·L-1·s-1
mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com