
【题目】在一定温度下将3 mol CO2和2 mol H2混合于2 L的密闭容器中,发生如下反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g)
CO(g)+H2O(g)
(1)该反应的化学平衡常数表达式K=________。
(2)已知在700 ℃时,该反应的平衡常数K1=0.6,则该温度下反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)的平衡常数K2=________,反应1/2CO2(g)+1/2H2(g)
CO2(g)+H2(g)的平衡常数K2=________,反应1/2CO2(g)+1/2H2(g) ![]() 1/2CO(g)+1/2H2O(g)的平衡常数K3=________。
1/2CO(g)+1/2H2O(g)的平衡常数K3=________。
(3)已知在1 000 ℃时,该反应的平衡常数K4为1.0,则该反应为________反应(填“吸热”或“放热”)。
(4)能判断该反应达到化学平衡状态的依据是________。(填编号)
A.容器中压强不变
B.c(CO2)=c(CO)
C.生成a mol CO2的同时消耗a mol H2
D.混合气体的平均相对分子质量不变
(5)在1 000 ℃下,某时刻CO2的物质的量为2.0 mol,则此时v正________v逆(填“>”、“=”或“<”)。该温度下反应达到平衡时,CO2的转化率为________。
【答案】(1)![]() ;(2)1.67,0.77;(3)吸热;(4)C;(5)>,40%。
;(2)1.67,0.77;(3)吸热;(4)C;(5)>,40%。
【解析】
试题(1)化学平衡常数:达到平衡,生成物浓度的幂之积与反应物浓度幂之积的比值,即K=![]() ;(2)K2=c(CO2)×c(H2)/[c(CO)×c(H2O)]=1·K-11=1.67,同理K32=K1,则K3=0.77;(3)化学平衡常数,受温度的影响,升高温度,平衡常数增大,说明向正反应方向进行,根据勒夏特列原理,正反应方向是吸热反应;(4)A、压强和物质的量成正比,因为反应前后气体的系数之和相等,反应始终,压强不变,因此不能说明达到平衡,故错误;B、投入量不同,系数相同,达到平衡时两者浓度不相等,故错误;C、不同物质的反应速率判断是否达到化学平衡,要求反应方向一正一逆,且速率之比为系数之比,生成CO2和消耗H2,反应方向一正一逆,转化都是amol,等于系数之比,因此能判断达到平衡状态,故正确;D、M=m/n,组分都是气体,气体的质量不变,反应前后气体系数相等,,因此M不变,不能作为达到平衡的标志,故错误;(5)1000℃下,CO2的物质的量为2mol,则H2、CO、H2O的物质的量为1mol,此时的浓度商Q=0.5<1,说明反应向正反应方向进行,即填写“>”,根据化学平衡常数,求出达到平衡时组分中CO2的物质的量为1.8mol,CO2的转化率为(3-1.8)/3×100%=40%。
;(2)K2=c(CO2)×c(H2)/[c(CO)×c(H2O)]=1·K-11=1.67,同理K32=K1,则K3=0.77;(3)化学平衡常数,受温度的影响,升高温度,平衡常数增大,说明向正反应方向进行,根据勒夏特列原理,正反应方向是吸热反应;(4)A、压强和物质的量成正比,因为反应前后气体的系数之和相等,反应始终,压强不变,因此不能说明达到平衡,故错误;B、投入量不同,系数相同,达到平衡时两者浓度不相等,故错误;C、不同物质的反应速率判断是否达到化学平衡,要求反应方向一正一逆,且速率之比为系数之比,生成CO2和消耗H2,反应方向一正一逆,转化都是amol,等于系数之比,因此能判断达到平衡状态,故正确;D、M=m/n,组分都是气体,气体的质量不变,反应前后气体系数相等,,因此M不变,不能作为达到平衡的标志,故错误;(5)1000℃下,CO2的物质的量为2mol,则H2、CO、H2O的物质的量为1mol,此时的浓度商Q=0.5<1,说明反应向正反应方向进行,即填写“>”,根据化学平衡常数,求出达到平衡时组分中CO2的物质的量为1.8mol,CO2的转化率为(3-1.8)/3×100%=40%。


科目:高中化学 来源: 题型:
【题目】向两个体积可变的密闭容器中均充入1mol的A2和2mol的B2发生反应:A2(g)+2B2(g)![]() 2AB2(g) △H。维持两个容器的压强分别为p1和p2,在不同温度下达到平衡,测得平衡时AB2的体积分数随温度的变化如图所示。
2AB2(g) △H。维持两个容器的压强分别为p1和p2,在不同温度下达到平衡,测得平衡时AB2的体积分数随温度的变化如图所示。
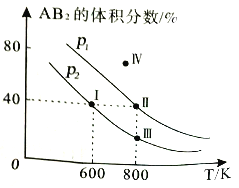
已知:图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上;IV点不在曲线上
下列叙述正确的是
A. Ⅰ点和Ⅱ点反应速率相等 B. IV点时反应未到达平衡v(正)<v(逆)
C. I点时,A的平衡转化率为40% D. 将点II所对应容器冷却到600K,可变成点I
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知40℃时水的离子积常数为Kw。该温度下, 将浓度为 a mol/L的一元酸HA与 b mol/L的一元碱BOH等体积混合,该溶液呈中性时,下列叙述不正确的是
A. a=b,pH=7
B. 混合溶液的c(H+)=c(OH-)
C. 混合溶液中,c(B+) =c(A-)
D. 混合溶液中,c(OH-)= ![]() mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的有效利用可以缓解温室效应和能源短缺问题。
(1)固态 CO2(干冰)所属晶体类型___________,所含化学键类型为__________(填“非极性键”或“极性键”或“离子键,下同)。CO2与Na2O2反应过程形成化学键类型为______________________________。
(2)中科院的科研人员在Na-Fe3O4和HMCM-22 的表面将CO2转化为烷烃,其过程如下图。
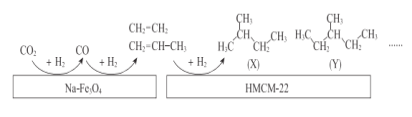
①Na-Fe3O4和HMCM-22 在反应中的作用为_______________。
②写出(X)的所有同分异构体结构简式_______________。
③关于X与Y的说法正确的是__________(填序号〕。
a.最简式相同 b.都有4种一氯代物
c.都易使酸性KMnO4溶液褪色 d.X与Y互称同系物
(3)同温同压下,蒸气密度是氢气15倍的烷烃(M),写出其与氯气反应生成一氯代烃的方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于消去反应的是 ( )
A.溴乙烷和氢氧化钠溶液混合加热
B.一氯甲烷与苛性钠的乙醇溶液混合共热
C.氯苯与氢氧化钠溶液混合加热
D.1—碘丁烷与氢氧化钾的乙醇溶液混合加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下的容积不变的容器中,当下列物理量不再变化时,表明反应A(g)+2B(g)![]() 3C(g)+D(s)已达到平衡的是( )
3C(g)+D(s)已达到平衡的是( )
① 混合气体的压强 ② 混合气体的密度
③ 混合气体的总质量 ④ 气体的总物质的量
A. ① ④B. ② ③C. ① ② ③D. ① ②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别向等体积1mol/L盐酸和1mol/L醋酸溶液中加入等量的镁条,反应时间与溶液pH变化关系如右图。下列说法中不正确的是( )

A. Y代表盐酸与镁条的反应
B. a点时反应Y消耗镁条的量少
C. b点表示此时两溶液pH相等
D. c点表示此时反应结束
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活息息相关,在各个方面都起着重要的作用。
(1)材料是经济和生态文明建设的重要物质基础。
合成塑料在生活中广泛应用,乙烯形成聚乙烯的方程式:_____________________。该反应的反应类型:_________________.橡胶是制造轮胎的重要原料,橡胶属于____________________填字母。
A金属材料 B无机非金属材料 C有机高分子材料
铝热反应在工业生产中的重要用途之一是焊接钢轨,其反应的化学方程式为:______________________________________;钢铁制品在潮湿的空气中能发生腐蚀,发生该腐蚀时的负极反应式为__________________________________。
(2)“三高症”是指高血糖糖尿病、高血脂和高血压症,是现代社会中的“富贵病”。
①血糖是指血液中的葡萄糖。葡萄糖的结构简式是__________________________。在加热条件下,加入氢氧化钠溶液,调节溶液为碱性,此时葡萄糖与新制的氢氧化铜发生反应,观察到的现象是________________此方法曾经用于检测糖尿病。
②血脂是血液中所含脂类物质的总称。油脂对人体的作用之一是________,但过量摄入,可能引起肥胖、高血脂、高血压。油脂在碱性条件下水解反应称为_____________.
③高血压可由肥胖、糖尿病、摄入过多钠盐等引起,而摄入过量的蛋白质也会造成脂肪堆积。蛋白质水解的最终产物是________,蛋白质的组成元素除C、H、O外,还含有_______(填一种)。
(3)石油在生活中的应用广泛。石油是由多种碳氢化合物组成的混合物,从原油中分离出汽油、煤油、柴油等轻质油的方法是____________________(填操作名称).分离出的汽油_______(填“是”或者“否”)可作萃取剂。汽油是C5~C11的混合烃,其中含有5个碳原子的烷烃存在________种同分异构体,其中一种同分异构体的一氯代物只有一种,则该同分异构体与氯气发生取代反应生成一氯代物的化学方程式为:___________________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com