
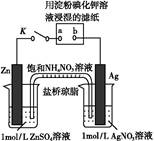
| A.Ag电极上发生氧化反应 |
B.盐桥中N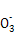 向Zn电极移动 向Zn电极移动 |
| C.电子沿Zn→a→b→Ag路径流动 |
| D.片刻后可观察到滤纸a点变蓝 |
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源:不详 题型:填空题
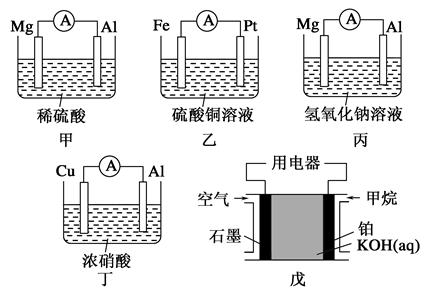
| 装置序号 | 正极 | 负极反应式 | 阳离子移动方向 |
| 甲 | | | |
| 乙 | | | |
| 丙 | | | |
| 丁 | | | |
| 戊 | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
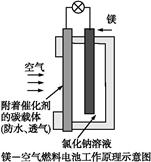
| A.该电池Mg作负极,发生还原反应 |
| B.该电池的正极反应式为:O2+2H2O+4e-=4OH- |
| C.电池工作时,电子通过导线由碳电极流向Mg电极 |
| D.当电路中通过0.2 mol电子时,消耗的O2体积为1.12 L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.把SO2通入紫色石蕊试液,可验证SO2的漂白性 |
B.构成如图所示装置时,盐桥中的K+向左池移动 |
| C.配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液浓度偏高 |
| D.将l0 克 ZnSO4·7H2O溶解在90克水中配制10%的ZnSO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
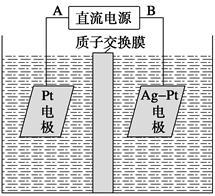
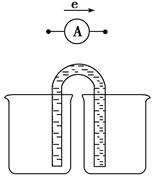
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
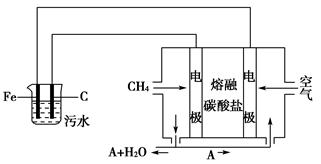
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
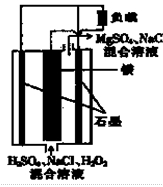
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
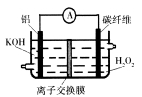
| A.铝作负极,电池工作时将不断溶解 |
| B.该电池不是二次电池,不可充电 |
| C.碳纤维电极的电极反应是H2O2+2 e一+2H+ =" 2" H2O |
| D.电池工作时OH一从碳纤维电极透过离子交换膜移向Al电极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com