
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是
A.甲的分子数比乙的分子数多
B.甲的物质的量比乙的物质的量小
C.气体摩尔体积:甲<乙
D.甲的相对分子质量比乙的相对分子质量小
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:2015-2016学年江苏省高二上学期期中选修化学试卷(解析版) 题型:选择题
合成氨的反应是:N2(g)+3H2(g) 2NH3(g);△H<0。使产率增大的方法是
2NH3(g);△H<0。使产率增大的方法是
A.升高温度 B.降低压强 C.使用催化剂 D.及时分离出NH3
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期期中测试化学试卷(解析版) 题型:选择题
已知还原性:Cl—<Br—<Fe2+<I—<SO2,由此判断下列反应必然发生的是
①2Fe3++SO2+2H2O=2Fe2++SO42—+4H+
②I2+SO2+2H2O=4H++ SO42—+2I—
③2Fe2++I2=2Fe3++2I—
④2Br—+4H++ SO42—=SO2↑+Br2+2H2O
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高一10月月考化学试卷(解析版) 题型:选择题
下列条件下,两瓶气体所含的原子数一定相等的是
①同质量不同密度的CO和N2
②同温同体积的H2和Cl2
③同体积同密度的O2和O3
④同压同体积的N2O和CO2
A.①③ B.①②
C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源:2016届山西怀仁第一中学高三上学期期中考试化学试卷(解析版) 题型:选择题
二氧化硒( SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。在回收过程中涉及如下化学反应:①SeO2 + 4KI + 4HNO3 =Se + 2I2 + 4KNO3 + 2H2O;②Se + 2H2SO4(浓) = 2SO2↑+ SeO2 + 2H2O;③Se + 4HNO3(浓) = SeO2 + 4NO2↑+ 2H2O。下列有关叙述正确的是
A.SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)>SeO2>I2
B.反应①中Se是氧化产物,I2是还原产物
C.反应①中生成0.6 mol I2,转移的电子数目为2.4NA
D.反应②、③中等量的Se消耗浓H2SO4和浓HNO3的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源:2015-2016河北石家庄第一中学高二上期中考试化学试卷(解析版) 题型:选择题
用铂电极电解100mL H2SO4 与CuSO4 的混合液,通电一段时间后,两极均收集到2.24L气体(标准状况),则原混合液中Cu2+的物质的量浓度为
A.1mol﹒L-1 B.2 mol﹒L-1 C.2.5 mol﹒L-1 D.3 mol﹒L-1
查看答案和解析>>
科目:高中化学 来源:2015-2016安徽蚌埠第二中学高二上学期期中考试化学试卷(解析版) 题型:推断题
根据图示填空:
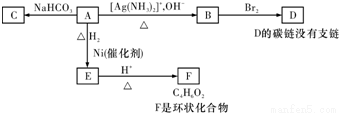
(1)化合物A含有的官能团是_________________________;
(2)1mol A与2mol H2反应生成1mol E,其反应方程式是_________________________;
(3)与A具有相同官能团的A的同分异构体的结构简式是________________________;
(4)B在酸性条件下与Br2反应得到D,D的结构简式是_____________________;
(5)F的结构简式是________________,由E生成F的反应类型是___________________;
(6)写出E在一定条件下发生反应生成高聚物的化学方程式___________________;
查看答案和解析>>
科目:高中化学 来源:2016届辽宁沈阳市高三上学期期中考试化学试卷(解析版) 题型:填空题
下图中A~J分别代表相关反应的一种物质,图中有部分生成物未标出。

已知:A分解得到等物质的量的B、C、D。
(1)A的化学式 ,B的结构式 。
(2)写出反应①的实验现象: 。
(3)写出反应③的离子方程式: 。
(4)写出反应⑤的化学方程式: 。
(5)常温常压下测得,1mol D发生反应②时,放出akJ热量,写出该反应的热化学方程式 。
(6)实验室检验气体D的常用方法及现象是 。
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三12月月考化学试卷(解析版) 题型:选择题
将KCl和CuSO4两种溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图所示,则下列说法正确的是
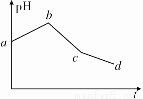
A.ab段表示电解过程中H+被还原,pH上升
B.电解开始时阳极先发生电极反应2Cl--2e-=Cl2↑
C.电解 至c点时,往电解液中加入适量CuCl2固体,即可使电解液
至c点时,往电解液中加入适量CuCl2固体,即可使电解液
恢复至原来的浓度
D.原混合溶液中KCl和CuSO4的浓度之比恰好为2∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com