
| A、C8H18(l)+12.5O2 (g)=8CO2 (g)+9H2O(l)△H=-5518 kJ?mol-1 |
| B、KOH(aq)+CH3COOH (aq)=CH3COOK(aq)+H2O(l)△H=-57.3 kJ?mol-1 |
| C、2H2(g)+O2(g)=2H2O(l)△H=-572kJ?mol-1 |
| D、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-533kJ?mol-1 |


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
A、N原子的最外层电子轨道表示式: | ||
B、质子数为35、中子数为45的溴原子:
| ||
C、硫离子的结构示意图: | ||
D、间二甲苯的结构简式: |
查看答案和解析>>
科目:高中化学 来源: 题型:
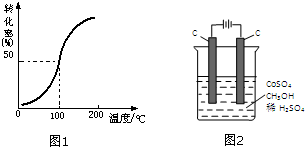 甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景.
甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景.| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1 452 kJ?mol-1 |
| B、CH3OH(l)+1.5O2(g)=CO2(g)+2H2O(g)△H=-725.8 kJ?mol-1 |
| C、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-725.8 kJ?mol-1 |
| D、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=+1 452 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、随着原子序数的递增,原子最外层电子总是从1到8重复出现 |
| B、元素的性质随着元素原子序数的递增而呈周期性变化 |
| C、随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 |
| D、元素性质的周期性变化是指原子核外电子排布的周期性变化、原子半径的周期性变化以及元素主要化合价的周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、V1>V2>V3 |
| B、V1>V3>V2 |
| C、V2>V3>V1 |
| D、V3>V1>V2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 且a、b、c、d均大于零,则下列说法正确的是( )
且a、b、c、d均大于零,则下列说法正确的是( )| A、断开1molH-Cl键所需的能量为-a-b-c |
| B、b>c,则氢气分子具有的能量高于氯气分子具有的能量 |
| C、Cl2(s)=Cl2(g)△H=+(a+d)kJ?mol-1 |
| D、向1molCl2(g)中通入1molH2(g),发生反应时放热dkJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
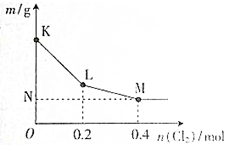 向100mlNaBr和NaI的混合溶液中慢慢通入Cl2(假设Cl2全部反应),使其充分反应后,将所得溶液蒸干、灼烧、得到的固体的质量为m,m与通入的n(Cl2)的关系如图所示,下列说法正确的是( )
向100mlNaBr和NaI的混合溶液中慢慢通入Cl2(假设Cl2全部反应),使其充分反应后,将所得溶液蒸干、灼烧、得到的固体的质量为m,m与通入的n(Cl2)的关系如图所示,下列说法正确的是( )| A、K→L段发生反应的离子方程式为2Br-+Cl2═2Cl-+Br2 |
| B、原溶液中,c(Na+ )=4mol?L-1 |
| C、原溶液中,c(I-)=2mol?L-1 |
| D、M点代表的固体质量为46.8g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 充电 |
| 放电 |
| A、构成该电池的正极和负极必须是两种活性不同的金属 |
| B、充电时有CH3OH生成的电极为阳极 |
| C、放电时负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O |
| D、充电时每生成1 mol CH3OH转移12mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com