
设NA为阿伏加德罗常数的值,N表示粒子数。下列说法正确的是
A.0.1 mol苯乙烯中含有碳碳双键的数目为0.4NA
B.将1molCl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2[NA—N(Cl2)]
C.一定条件下,0.1 mol SO2与足量氧气反应生成SO3,转移电子数为0.2NA
D.电解精炼铜,当电路中通过的电子数目为0.2NA时,阳极质量减少6.4g
科目:高中化学 来源:2014-2015河北唐山市高一下学期开学调研考试化学试卷(解析版) 题型:选择题
下表各选项中,通过置换反应不能实现由Y到W转化的一组化合物是
A. | B. | C. | D. | |
Y | Na2CO3 | SiO2 | Fe2O3 | H2O |
W | NaHCO3 | CO | Al2O3 | NaOH |
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省唐山市高二下学期开学调研化学试卷(解析版) 题型:选择题
反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在2升密闭容器中进行1分钟后,NH3减少了0.12 mol,则平均每秒钟浓度变化正确的是
A.H2O:0.002 mol·L-1 B.NO:0.001 mol·L-1
C.NH3: 0.002 mol·L-1 D.O2:0.0025 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河东区高三一模理综化学试卷(解析版) 题型:选择题
高铁酸盐在能源环保领域有广泛用途。用镍(Ni),铁做电极电解浓氢氧化钠溶液制备Na2FeO4的装置如图,说法合理的是

A.镍是阳极,电极反应4OH--4e-=2H2O+O2↑
B.电解时电流方向:负极→镍电极→溶液→铁电极→正极
C.若隔膜是阴离子交换膜,则OH-自右向左移动
D.电解时阳极区pH降低,阴极区pH升高,撤去隔膜后与原溶液比较pH降低(假设电解前后体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省宜宾市高三第二次诊断测试化学试卷(解析版) 题型:推断题
(14分)苯丙醇胺 是一种人工合成的药品制剂,英文名称是Phenylpropanolamine,缩写为PPA,结构简式如图所示,其合成路线如下:
是一种人工合成的药品制剂,英文名称是Phenylpropanolamine,缩写为PPA,结构简式如图所示,其合成路线如下:

其中A~F分别代表一种有机化合物,合成路线中部分产物及反应条件已略去。已知:

请回答下列问题:
(1)PPA的分子式是 ;F中官能团的名称是 。
(2)E的结构简式是 ;烃A的核磁共振氢谱有 种峰。
(3)上述合成路线中属于加成反应的是 。(填数字序号)
(4)第②步的化学方程式是 。
(5)E的一种同分异构体在一定条件下能发生缩聚反应,该反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省广安市高三二诊理综化学试卷(解析版) 题型:简答题
(16分) 研究发现铜具有独特的杀菌功能, 能较好地抑制病菌的生长。现有工业上由辉铜矿石(主要成分Cu2S)的冶炼铜两种方案:
Ⅰ 火法炼铜在1200℃发生的主要反应为:
①2Cu2S+3O2=2Cu2O+2SO2 ②2Cu2O+Cu2S= 6Cu+SO2↑
此方案的尾气可以用表中方法处理
方法1 | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫,其部分热化学方程式为: 2CO(g)+SO2(g)= S(g)+2CO2(g) ΔH=+8. 0 kJ·mol-1 2H2(g)+SO2(g)= S(g)+2H2O(g) ΔH=+90. 4 kJ·mol-1 |
方法2 | 用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸
|
Ⅱ“细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如溶液中亚铁硫杆菌能利用空气中的氧气将黄铁矿(主要成分FeS2)氧化为Fe2(SO4)3,并使溶液酸性增强;利用Fe2(SO4)3作氧化剂溶解辉铜矿石,溶液酸性又进一步增强,过滤未溶解完的辉铜矿石,在滤液中加入足量的铁屑,待反应完全后过滤出铜和剩余的铁屑,得溶液Xml(设整个过程中其它杂质不参与反应,不考虑溶液离子水解)。其流程如图:

(1)Ⅱ相对于Ⅰ的优点是______________________________。(说一点即可)
(2)Ⅰ中反应2Cu2O+Cu2S= 6Cu+SO2↑氧化剂是________
(3)已知CO的燃烧热283. 0 kJ·mol-1,写出S(g)与O2(g)反应生成SO2(g)的热化学方程式___________。
(4)若用Ⅰ中方法2吸收尾气,则开始时阳极的电极反应式为________________。
(5)写出Ⅱ中黄铁矿氧化过程的化学反应方程式______________________________
(6)假设Ⅱ中每一步都完全反应,消耗掉标况下空气5×22.4VL(氧气体积分数为20%),则所得c(Fe2+)=________________(可以写表达式)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省广安市高三二诊理综化学试卷(解析版) 题型:选择题
下列有关实验操作及现象与相应结论都正确的是
选项 | 实验操作及现象 | 实验结论 |
A | 将Cl2通入品红溶液中,品红溶液褪色 | 证明Cl2有还原性 |
B | 蔗糖溶液在硫酸存在下水浴加热一段时间后,再与银氨溶液混合水浴加热,无银镜出现 | 蔗糖没有水解 |
C | 向鸡蛋清溶液中加入饱和硫酸铵溶液,有白色沉淀生成 | 蛋白质变性 |
D | 铝箔在酒精灯火焰上,加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三第一次模拟考试理综化学试卷(解析版) 题型:填空题
选做(12分)【化学一化学与技术】海水资源丰富,海水中主要含有Na+、K+、Mg2+、Cl-、 、Br-、
、Br-、 、
、 等离子。
等离子。
合理利用海水资源和保护环境是我国可持续发展的重要保证。
I.火力发电燃煤排放的SO2会造成一系列环境和生态问题。利用海水脱硫是一种有效的方法,其工艺流程如下图所示:

(1)天然海水的pH≈8,呈弱碱性。用离子方程式解释原因___________________________。
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是_______。氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是___________________________________________________________________________。
Ⅱ.重金属离子对河流及海洋造成严重污染。某化工厂废水(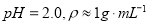 )中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol·L-1。排放前拟用沉淀法除去这两种离子,查找有关数据如下:
)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol·L-1。排放前拟用沉淀法除去这两种离子,查找有关数据如下:

(3)你认为往废水中投入_________(填字母序号),沉淀效果最好。
A.NaOH B.Na2S C.KI D.Ca(OH)2
(4)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中 ________。
________。
(5)如果用食盐处理其只含Ag+的废水,测得处理后废水中NaCl的质量分数为0.117%。
若环境要求排放标准为c(Ag+)低于1.0×10-8mol·L-1,问该工厂处理后的废水中c(Ag)+=__________,是否符合排放标准__________(填“是”或“否”)。已知Ksp(AgCl)=1.8×10-10mol2·L-2。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东肥城市高三一模理综化学试卷(解析版) 题型:填空题
(16分)CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径。
(1)下图是在101 kPa,298 K条件下1 mol NO2和1 mol CO反应生成1 mol CO2和1 mol NO过程中能量变化示意图。
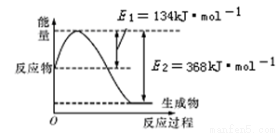
已知:①N2 (g) +O2 (g) =2 NO (g) ΔH=179.5 kJ·mol—1
②2NO (g) +O2 (g) =2 NO2 (g) ΔH=—112.3 kJ·mol—1
请写出NO与CO反应生成无污染气体的热化学方程式:_____________________。
(2)工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=—49.0 kJ·mol—1
CH3OH(g)+H2O(g) ΔH=—49.0 kJ·mol—1
某科学实验小组将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标)。
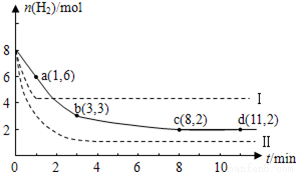
①该反应在0 ~8 min内CO2的平均反应速率是_____________________;
②该反应的平衡常数表达式为:K=_____________________;
③仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。与实线相比,曲线Ⅰ改变的条件可能是_____________________,曲线Ⅱ改变的条件可能是____________________。若实线对应条件下平衡常数为K,曲线Ⅰ对应条件下平衡常数为K1,曲线Ⅱ对应条件下平衡常数为K2,则K、K1和K2的大小关系是_____________________;
(3)有学者设想以如图所示装置用电化学原理将他们转化为重要化工原料。请回答:
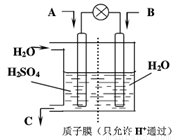
①若A为SO2,B为O2,C为H2SO4,则负极反应式___________________;
②若A为CO2,B为H2,C为CH3OH,则正极反应式__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com