
【题目】下图所涉及的物质均为中学化学中的常见物质,其中C、D均为气体单质,E是固体单质,A物质的焰色反应火焰为紫色,F是黑色晶体,它们存在如图转化关系,反应中生成的水及次要产物均的已略去。

(1)写出下列物质的化学式:C_______________,D_________________,H___________。
(2)指出MnO2在相关反应中的作用:反应①中做_______剂,反应②中做_________剂。
(3)当①中有1molA完全反应时转移电子的物质的量是________mol。
【答案】 O2 Cl2 FeCl3 催化(剂) 氧化(剂) 6
【解析】与MnO2反应的制备的气体有O2和Cl2,A物质的焰色反应火焰为紫色,F是黑色晶体,A和MnO2制备O2,在加热条件下用浓盐酸和MnO2制备Cl2,则A为KClO3,B为HCl,C为O2,D为Cl2,F为金属氧化物,与盐酸反应生成两种氯化物,且二者之间可以相互转化,说明E为变价金属,应为Fe,是目前人类应用最广泛的金属,则F为Fe3O4,G为FeCl2,H为FeCl3。
(1)写出下列物质的化学式:C: O2,D:Cl2,H:FeCl3。(2)指出MnO2在相关反应中的作用:在不加热条件下,用H2O2和MnO2制备O2,反应①中做催化剂;在加热条件下用浓盐酸和MnO2制备Cl2,MnO2中锰元素由+4价,降为+2,在反应②中做氧化剂。(3)根据化合价变化判断,已知:2KClO3![]() 2KCl+3O2↑,2molKClO3转移12mol电子,当①中有1molA即KClO3完全反应时转移电子的物质的量是6mol。
2KCl+3O2↑,2molKClO3转移12mol电子,当①中有1molA即KClO3完全反应时转移电子的物质的量是6mol。


科目:高中化学 来源: 题型:
【题目】10mL NO、CO2的混合气体通过足量的Na2O2后,气体的体积变为5mL(相同状况),则CO2和NO的体积比不可能为( )
A.1:1
B.2:1
C.3:2
D.1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.如图所示为常见玻璃仪器的部分结构:
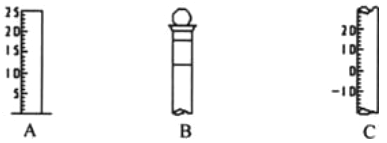
(1)请写出所列仪器的名称: A______,B_______,C_______;
(2)仪器 B 上标记有________(填序号);
①质量 ②温度 ③刻度线 ④浓度 ⑤容积
(3)仪器 B 使用前必须__________________。
II.已知某“84 消毒液”瓶体部分标签如图所示,该“84 消毒液”通常稀释 100 倍(体积之比)后使用。请回答下列问题:
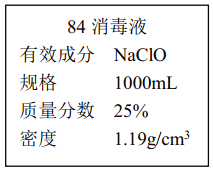
(1)该“84 消毒液”的物质的量浓度约为________mol·L-1。(保留两位有效数字)
(2)某同学取 100 mL 该“84 消毒液”,稀释后用于消毒,稀释后的溶液中 c(Na+)=________ mol·L-1。
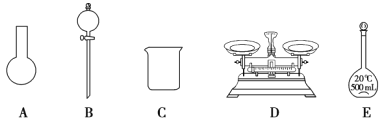
(3)该同学参阅该“84 消毒液”的配方,欲用 NaClO 固体配制 250 mL含 NaClO 质量分数为 25%的消毒液。下列说法不正确的是________(填序号)。
a.如图所示的仪器中,有三种是不需要的,还需要其它玻璃仪器
b.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
c.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
(4)“84 消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用 98%(密度为1.84g·cm-3)的浓硫酸配制2 000 mL 2.3 mol·L-1 的稀硫酸用于增强“84 消毒液”的消毒能力。需用浓硫酸的体积为________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
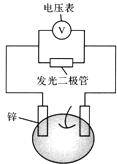
【题目】留心处处皆学问.从生活出发进行科学探究,可以获得自信,形成正确的思维方式.甲、乙两位同学一起合作设计完成了水果电池的实验(如图),测得数据如下
实验序号 | 电极材料 | 水果种类 | 电极间距离/cm | 电压/mV |
1 | 锌铜 | 菠萝 | 3 | 900 |
2 | 锌铜 | 苹果 | 3 | 650 |
3 | 锌铜 | 柑橘 | 3 | 850 |
4 | 锌铜 | 西红柿 | 3 | 750 |
5 | 锌铝 | 菠萝 | 3 | 650 |
6 | 锌铝 | 苹果 | 3 | 450 |
对甲同学提出的问题,乙同学的解释不正确的是( )
甲同学 | 乙同学 | |
A | 实验6中负极电极反应式如何写? | Al﹣3e﹣=Al3+ |
B | 实验1,5中电流方向为什么相反? | 1中锌为负极,电流由铜经导线流向锌,5中铝为负极,铝失去电子,电流由锌经导线流向铝 |
C | 水果电池的电压与哪些因素有关? | 只跟水果的类型有关 |
D | 实验中发光二极管不亮,如何使它亮起来 | 可用铜锌作电极,用菠萝作介质,并将多个此电池串联起来 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是
A.SO2水溶液呈酸性,可用于漂白纸浆B.晶体硅熔点高,可制半导体材料
C.Al(OH)3呈弱碱性,可用于治疗胃酸过多D.H2O2具有还原性,可用于消毒杀菌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5.1g镁、铝混合物溶于500mL1mol/L硫酸溶液中,充分反应共产生标况下VL氢气,向剩余溶液中逐滴滴加某氢氧化钠溶液至过量,这一过程中产生沉淀的物质的量与加入氢氧化钠溶液体积的关系如下图所示,请根据图中数据回答下列问题。(请书写必要的计算过程)
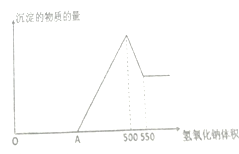
(1)氢氧化钠溶液的浓度是多少摩每升?_____________
(2)原固体混合物中铝的质量是多少克?__________________
(3)氢气的体积V是多少升?______________
(4)图中A点对应氢氧化钠溶液的体积是多少毫升?________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B的结构简式如图: 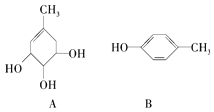
(1)A分子中含有的官能团的名称是;B分子中含有的官能团的名称是 .
(2)A能否与氢氧化钠溶液反应;B能否与氢氧化钠溶液反应 .
(3)A在一定条件下可得到B,其反应类型和条件分别是、 .
(4)A、B各1mol分别加入足量溴水,完全反应后消耗单质溴的物质的量分别是mol,mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知温度T时,水的离子积常数为Kw,该温度下,将浓度为a molL﹣1的一元酸HA溶液与b molL﹣1的一元碱BOH溶液等体积混合,可判断该溶液一定呈中性的依据是( )
A.混合溶液的PH=7
B.混合溶液中,C(H+)= ![]() mol?L﹣1
mol?L﹣1
C.a=b
D.混合溶液中,C(H+)+C(B+)=C(OH﹣)+C(A﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃,101kPa条件下,将15L O2通入10LCO和H2的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强.
(1)若剩余气体的体积是15L,则原CO和H2的混合气中V(CO)=L,V(H2)=L.
(2)若剩余气体的体积为a L,则原CO和H2的混合气中V(CO):V(H2)= .
(3)若剩余气体的体积为aL,则a的取值范围是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com