



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ |
| SO2 |
| A��MFe2Ox�������� |
| B��x��y |
| C��SO2�Ǹ÷�Ӧ�Ĵ��� |
| D��SO2����������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���� | B���ڢ� | C���٢� | D���٢ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ||
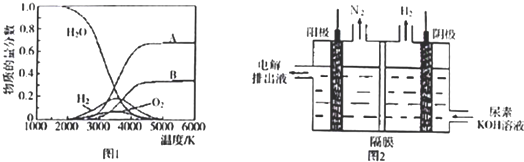
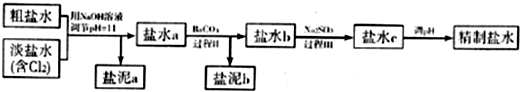
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��3mol NO2����H2O ��Ӧ��ת�Ƶ���2mol |
| B��1 mol C5H12 �����к��еĹ��ۼ���ĿΪ17N A |
| C��Ũ�Ⱦ�Ϊ0��lmol/L CH3COONa��CH3COOH �����Һ100mL ������CH3COO-��CH3COOH �Ļ�������Ϊ0.02NA |
| D����״����11.2L ��CH4��CD4��CT4�Ļ�������к��е�������Ϊ5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����������ѧ��������CO2��Ӧ���о���ȡ����һЩ��Ҫ�ɹ���
����������ѧ��������CO2��Ӧ���о���ȡ����һЩ��Ҫ�ɹ���| 3 |
| 2 |
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��������Ӧ���漰��������ԭ��Ӧ����3�� |
| B�������ԣ�Cl2��NaBi03��Bi205��Bi203? |
| C������NaBi03�ķ�Ӧ�У�NaBi03�Ļ�ѧ������Ϊ2 |
| D���õ�0.05molBi203ʱ�����������й�ת�Ƶ���0.4 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com