
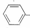
 一R能被酸性 KMn04溶液氧化生成
一R能被酸性 KMn04溶液氧化生成 一C00H,但若烷基 R中直接与苯环相连的碳原子上没有 C-H键,则不能被氧化得到一C00H. 现有分子式为 C11H16的一烷基取代苯,则它可以被氧化成为
一C00H,但若烷基 R中直接与苯环相连的碳原子上没有 C-H键,则不能被氧化得到一C00H. 现有分子式为 C11H16的一烷基取代苯,则它可以被氧化成为 一C00H 的同分异构体数目为( )
一C00H 的同分异构体数目为( )| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
分析 由题意可知,该苯的同系物的各同分异构体的苯环上都只有一个侧链,在写其同分异构体时,可以把苯环看作是C5H12的一个取代基,这样只要写出C5H12的3种同分异构体,结合烷基R中直接与苯环连接的碳原子没有C-H键,则不容易被氧化得到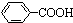 来解答.
来解答.
解答 解:由题意可知,该苯的同系物的各同分异构体的苯环上都只有一个侧链,在写其同分异构体时,可以把苯环看作是C5H12的一个取代基,这样写出C5H12的3种异构体:CH3CH2CH2CH2CH3、CH3CH(CH3)CH2CH3、C(CH4)2,其一取代苯共有7种异构体.分别是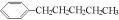 、
、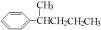 、
、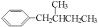 、
、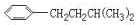 、
、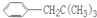 、
、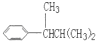 、
、 .故选B.
.故选B.
点评 本题考查有机物的结构与性质,注意苯环可以看做取代基,难度不大.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ②③④ | C. | ②③⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
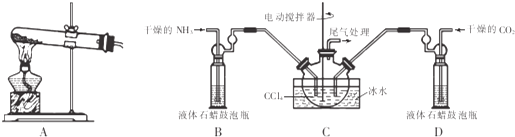
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
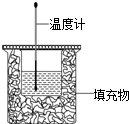 50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题:
50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
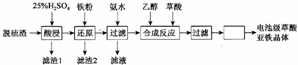
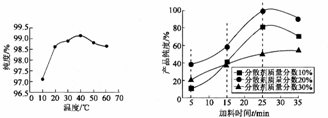
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
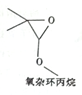
| A. | 该有机物能与金属钠反应 | |
| B. | 该有机物的分子式为C5H9O2 | |
| C. | 该有机物的同分异构体(不考虑立体异构)中,属于羧酸的物质共有5种 | |
| D. | 该有机物的同分异构体(不考虑立体异构体)中,能水解生成羧酸与醇的物质共有9种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com