
����Ŀ���¶�ΪTʱ����VL���ܱ������г���һ������A��B��������Ӧ��A(g)��B(g)![]() C(s)��xD(g) ��H��0��������A��B��D�����ʵ���Ũ����ʱ��ı仯����ͼ��ʾ������˵���в���ȷ����
C(s)��xD(g) ��H��0��������A��B��D�����ʵ���Ũ����ʱ��ı仯����ͼ��ʾ������˵���в���ȷ����

A.��Ӧ��ǰ10min��B���ʱ�ʾ��ƽ����Ӧ����v(B)��0.15 mol��L��1��min��1
B.�÷�Ӧ����ʽ�е�x��2
C.��ƽ��ʱ�����¶Ȳ��䣬ѹ�������ݻ���ƽ�����淴Ӧ�����ƶ�
D.��Ӧ��15minʱ���ı�������ǽ����¶�
���𰸡�C
��������
A. ��Ӧ��ǰ10min��B���ʱ�ʾ��ƽ����Ӧ����![]() (B) ��
(B) ��![]() 0.15 mol��L��1��min��1����A��ȷ��
0.15 mol��L��1��min��1����A��ȷ��
B. ��Ӧ����ʽ�����ʵı仯���ȵ���ϵ���ȣ�![]() ���÷�Ӧ����ʽ�е�x��2����B��ȷ��
���÷�Ӧ����ʽ�е�x��2����B��ȷ��
C. x��2����Ӧǰ������ϵ���Ͳ��䣬��ƽ��ʱ�����¶Ȳ��䣬ѹ�������ݻ���ƽ�ⲻ�ƶ�����C����
D. A(g)��B(g)![]() C(s)��2D(g) ����Ӧ���ȣ�����ͼ���֪����Ӧ��15minʱ��ƽ�������ƶ������Ըı�������ǽ����¶ȣ���D��ȷ��
C(s)��2D(g) ����Ӧ���ȣ�����ͼ���֪����Ӧ��15minʱ��ƽ�������ƶ������Ըı�������ǽ����¶ȣ���D��ȷ��
��ѡC��


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ظ������ˮ��Һ�д�������ƽ�⣺2CrO42-����ɫ��+2H+![]() Cr2O72-���Ⱥ�ɫ��+H2O������˵����ȷ����
Cr2O72-���Ⱥ�ɫ��+H2O������˵����ȷ����
A. ����Һ��pH����ʱ��ƽ�������ƶ�
B. �����£���������Һ������ˮϡ�͵�ԭ�����2����ƽ�������ƶ�
C. ����Һ��ɫ����ʱ����Һ��c(H+)/c(OH-)��һ����ֵ
D. ����CrO42-Ũ�ȣ�ƽ�������ƶ���ƽ�ⳣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѧ����ŵʵ������ֻ����Ƶ�һ����Ӧ�����÷�Ӧ�����������ѹ���ͺ�������ԭ����ʹ���ɻ�ѧʵ�����η�������ͼ��һ������ѧ����ŵʵ������
��֪����Cu2++4NH3H2O=4H2O+[Cu(NH3)4]2+(�÷�Ӧ�������ΪH2O2�Ĵ�������
����֪����A��C��Һ������Ũ����ͬ��ʵ��������п����ȫ��ͬ
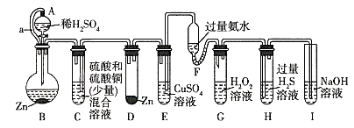
�����йط���������ǣ� ��
A.��ʵ��ɹ�����Ҫ����������װ������������
B.B�з�Ӧ���ʴ���D�з�Ӧ����
C.A��B֮�䵼��a��������ƽ��A��B����ѹ
D.H�г���dz��ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ú�Ļ��������У����dz�����Ҫ�о���ͬ�¶��µ�ƽ�ⳣ����Ͷ�ϱȼ����ʵ����⡣��֪CO(g)��H2O(g) ![]() H2(g)��CO2(g)��ƽ�ⳣ�����¶ȵı仯���±���
H2(g)��CO2(g)��ƽ�ⳣ�����¶ȵı仯���±���
�¶�/�� | 400 | 500 | 830 | 1 000 |
ƽ�ⳣ��/K | 10 | 9 | 1 | 0.6 |
�Իش��������⣺
��1��������Ӧ������Ӧ��___________��Ӧ(����ȡ������ȡ�)��
��2��ij�¶��£�������Ӧ�ﵽƽ���������������������¶ȣ�����Ӧ����_________(���������С�����䡱)�������ڻ�������ѹǿ___________(���������С�����䡱)��
��3��830 ��ʱ���ں��ݷ�Ӧ���з���������Ӧ�����±��е����ʵ���Ͷ�뷴Ӧ��������������Ӧ������е���_______________(ѡ����ĸ)��
Ͷ�� | A | B | C | D |
n(CO2)/mol | 3 | 1 | 0 | 1 |
n(H2)/mol | 2 | 1 | 0 | 1 |
n(CO)/mol | 1 | 2 | 3 | 0.5 |
n(H2 | 5 | 2 | 3 | 2 |
��4����830 ��ʱ����2 L���ܱ������м���4 mol CO(g)��6 mol H2O(g)��2min�ﵽƽ��ʱ��CO��ת����Ϊ____________����CO2��ʾ��ƽ����Ӧ����V(CO2)Ϊ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���ѧ���ںϳɰ���N2+3H2![]() 2NH3��H<0����Ӧ�����о���ȡ���½�չ���״α�����LiH-3d���ɽ�����һ���ϴ�����ϵ�������������ת��������������ͼ��ʾ������˵������ȷ����
2NH3��H<0����Ӧ�����о���ȡ���½�չ���״α�����LiH-3d���ɽ�����һ���ϴ�����ϵ�������������ת��������������ͼ��ʾ������˵������ȷ����
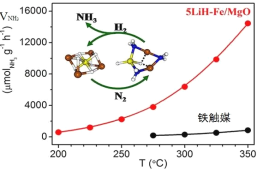
A.ת���������зǼ��Լ��������γ�
B.���ϴ��������˷�Ӧ�Ļ��
C.���ϴ����ܽ��ͺϳɰ���Ӧ���ʱ�
D.�����ºϳɰ��������ԭ��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ȼ�ϵ�ؾ��������ܶȽϸߺ�����Ⱦ���ص㣬�乤��ԭ������ͼ��ʾ������˵������ȷ����

A.������Ӧ��N2H4��4e����4H����N2��
B.ͨ�������ĵ缫Ϊ����
C.��ع���ʱOH�����ƶ�
D.�õ�ع���һ��ʱ��������Һ���Բ���(�����ǵ������Һ������仯)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ���й����ʵ���Ũ�ȹ�ϵ����ȷ����
A.pH��ȵ�NaOH��CH3COONa��NaHCO3������Һ������c(NaOH)<c(CH3COONa)<c(NaHCO3)
B.��֪25��ʱKsp(AgCl)��1.8��10��10������0.3 mol��L��1 NaCl��Һ�У�Ag�������ʵ���Ũ�����ɴﵽ6.0��10��10 mol��L��1
C.25��ʱ��0.1 mol��L��1 Na2CO3��Һ��ˮ���������c(OH)����0.1 mol��L��1 NaOH��Һ��ˮ���������c(OH��)
D.Ũ�Ⱦ�Ϊ0.1 mol/L��CH3COOH��CH3COONa��Һ�������ϣ�c(CH3COO��)��2c(OH��)��c(CH2COOH)��2c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA�ǰ����ӵ�������ֵ������˵����ȷ���ǣ� ��
A.11g��̬��ԭ�Ӻ��е�δ�ɶԵ�����Ϊ3NA
B.1mol��̬��ԭ��������ߵ��ܼ��ϵ�����Ϊ7NA
C.100mL1molL-l����������Һ���е���������Ŀ����0.1NA
D.��ⷨ����ͭ����������64gCuʱ������ת�Ƶĵ���������2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С��Ϊ̽���������������������绯ѧ��ʴ�����ͼ���ʴ���ʣ�����Ͼ��ȵ��������ۺ�̼��������ƿ�ײ�������ƿ������ͼ 1 ��ʾ�� �ӽ�ͷ�ι��е��뼸�δ�����Һ��ͬʱ���������е�ѹǿ�仯��
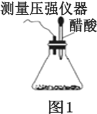
��1�����������ʵ����ƣ���ɱ��пո�
��� | ʵ��Ŀ�� | ̼��/g | ����/g | ����/% |
�� | Ϊ����ʵ�������� | 0.5 | 2.0 | 90.0 |
�� | ______________ | 0.5 | ____________ | 36.0 |
�� | ̼�ۺ�����Ӱ�� | 0.2 | 2.0 | 90.0 |
��2����Ţ�ʵ����������ѹǿ��ʱ��仯��ͼ 2�� t2 ʱ��������ѹǿ����С����ʼѹǿ�� ��ԭ������������_____��ʴ�� ����ͼ 3 ���ü�ͷ��������ø�ʴʱ������������_____����ʱ��̼�۱��淢����_____(���������ԭ��)��Ӧ����缫��Ӧʽ��_____��
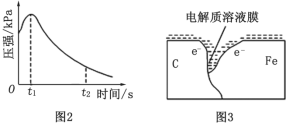
��3����С���ͼ 2 �� 0��t1 ʱѹǿ����ԭ����������¼��裬������ɼ������
����һ���������ⸯʴ���������壻
�������_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com