
| 浓硫酸 |
| 密度(g/mL) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 冰醋酸 | 1.049 | 16.6 | 118.1 | 能溶于水 |
| 异戊醇 | 0.812 | -117.2 | 130.5 | 微溶于水 |
| 乙酸异戊酯 | 0.869 | -78 | 140 | 难溶于水 |
| 实际产量 |
| 理论产量 |
| 8.4 |
| 11.96 |


 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 探究内容 | 实验方案 | 实验现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、△H4=
| ||
B、△H4=
| ||
C、△H4=
| ||
D、△H4=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| C | 二氧化硫通入品红溶液中 | 品红溶液褪色 | 二氧化硫具有还原性 |
| D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
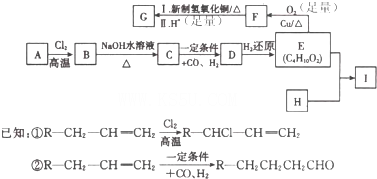
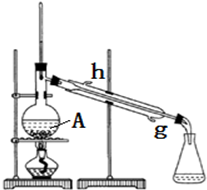
查看答案和解析>>
科目:高中化学 来源: 题型:
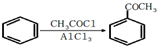 ,请结合题中所给信息,写出由CH3CH2COOH、为原料合成
,请结合题中所给信息,写出由CH3CH2COOH、为原料合成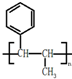 的合成路线流程图(无机试剂任选).合成路线流程图示例:H2C=CH2
的合成路线流程图(无机试剂任选).合成路线流程图示例:H2C=CH2| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验事实 | 结论 | |
| A | Cl2的水溶液可以导电 | Cl2是电解质 |
| B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
| C | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 结合H+的能力:CO32-<AlO2- |
| D | 常温下白磷可自燃,而氮气须在放电时才与氧 气反应 | 非金属性:P>N |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com