
分析 (1)①石蕊试纸检验气体需要湿润;
②容量瓶需要检查是否漏液;
(2)A.先移出导管,后撤酒精灯,可防止水倒流;
B.给试管加热时,先均匀加热,后局部加热,防止受热不均匀;
C.中和减低腐蚀性;
D.浓硫酸不能用水冲洗,稀释放出大量的热;
E.点燃可燃性气体(如H2、CO、C2H4等)时,若不纯易发生爆炸.
解答 解:(1)①石蕊试纸(检验气体性质)第一步操作为将石蕊试纸润湿,故答案为:将石蕊试纸润湿;
②容量瓶使用的第一步操作为检验容量瓶是否漏水,故答案为:是否漏水;
(2)A.先移出导管,后撤酒精灯,可防止水倒流试管炸裂,操作合理,故A正确;
B.给试管加热时,先均匀加热,后局部加热,防止受热不均匀,操作合理,故B正确;
C.碱液流到桌子上,先用稀醋酸溶液中和,后用水洗,减低腐蚀性,操作合理,故C正确;
D.浓硫酸不能用水冲洗,稀释放出大量的热,不能立即用水冲洗,先用布擦拭,再用水冲洗,后涂上3%-5%的NaHCO3溶液,故D错误;
E.点燃可燃性气体(如H2、CO、C2H4等)时,若不纯易发生爆炸,则先检验气体纯度,后点燃,故E正确;
故答案为:ABCE.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、实验基本操作、实验安全为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:解答题
| 25℃ | pH | 25℃ | pH |
| 饱和H2S溶液 | 3.9 | FeS开始沉淀 | 3.0 |
| SnS沉淀完全 | 1.6 | FeS沉淀完全 | 5.5 |
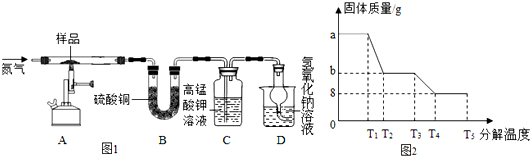
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②⑤⑥ | C. | ①②④⑤ | D. | ②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
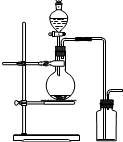
| A. | 氯酸钾溶液与二氧化锰反应制氧气 | B. | 浓氨水与氢氧化钙固体制氨气 | ||
| C. | 乙醇和浓硫酸(170℃)制乙烯 | D. | 铜和浓硝酸制二氧化氮 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O4的摩尔质量是64g | |
| B. | O4与O3、O2互为同位素 | |
| C. | 相同质量的O4与O3所含原子个数之比为1:1 | |
| D. | 32gO4所含的电子数为32NA(NA为阿伏加德罗常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸和氯水用棕色试剂瓶保存 | |
| B. | 硫化钠和硫酸亚铁固体长期暴露在空气中变质 | |
| C. | 常温下铁和铂都不溶于浓硝酸 | |
| D. | H2O2溶液中加入少量MnO2或FeCl3溶液都能增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
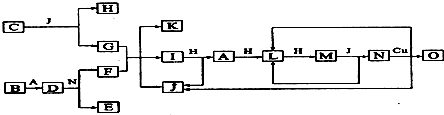
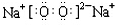 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com