
(1)已知标准状况下11.2L X气体的质量为16g ,则该X气体的物质的量为 ,其摩尔质量为 ;
(2)12.4 g Na2X中含Na+ 0.4 mol,则Na2X的摩尔质量是 ,X的相对原子质量是 。
(3).由CH4和CO组成的混合气体,在标准状况下的平均密度为0.848g/L,则该混合气体的平均摩尔质量为 ,混合气体中CH4和CO的物质的量之比为 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
对于易燃、易爆、有毒的化学物质,往往会在其包装上贴上危险警告标签。下面所列的物质中,标签贴错了的是( )
| A | B | C | D | |
| 物质的化学式 | 浓H2SO4 | 汽油 | 乙醇 | KNO3 |
| 危险警告标签 |
|
|
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量相等的CO和CO2 的下列比较中正确的是( )
① 所含的分子数目之比为1︰1 ② 所含的O原子数目之比为1︰2
③ 所含的原子总数目之比为2︰3 ④ 所含的C原子数目之比为1︰1
⑤ 所含的电子数目之比为7︰11
A.①② B.②③ C.①②③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有较大量的Cl-、CO32-、OH-等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出,下列实验操作顺序正确的是 ( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.①②④②③ B.④②①②③ C.①②③②④ D.④②③②①
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.0.5mol O3 和11.2L O2的体积一定相等
B.标准状况下,11.2L 水中含有分子的数目为0.5NA
C.常温常压下,18g H2O含有的原子总数为3NA
D.2.8g CO和N2混合气体中含有的原子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A(g)+3B(g)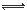 2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是
A.υ(D)=0.4 mol / (L·s) B.υ(C)=0.5 mol / (L·s)
C.υ(B)=0.6 mol / (L·s) D.υ(A)=0.15 mol / (L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2CO(g)+O2(g)=2CO2(g) ΔH= -566 kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+ 1/2O2(g) ΔH= -226 kJ/mol
根据以上热化学方程式判断,下列说法正确的是
A.CO的燃烧热为566 kJ/mol
B.右图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
D.CO2(g)与Na2O2(s)反应放出452kJ热量时,电子转移的物
质的量为为2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法或表示正确的是( )
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.物质发生化学变化时一定伴随着吸热现象或放热现象
C.稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含l mol NaOH的溶液混合,放出的热量大于57.3kJ
D.在25℃101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ的热量,则H2燃烧的热化学方程式为:2H2(g)+O2(g)====2H2O(l); △H=-285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关阿佛加德罗常数(NA)的说法错误的是( )
A.32gO2所含的原子数目为NA B.0.5molH2O含有的原子数目为1.5NA
C.1molH2O含有的H2O分子数目为NA D.0.5NA个氯气分子的物质的量是0.5mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com