
【题目】室温下,用0.100mol/L NaOH溶液分别滴定20.00mL 0.100mol/L的盐酸和醋酸。下列说法正确的是
A.起始时盐酸和醋酸溶液的pH相同
B.V(NaOH)=10.00mL时,醋酸溶液中,![]()
C.恰好中和时,两种酸所用NaOH溶液体积不相等,醋酸用的体积少
D.V(NaOH)=20.00mL时,c(Cl-)>c(CH3COO-)
【答案】D
【解析】
A.醋酸是弱电解质,部分电离,0.100 mol/L的盐酸和醋酸,后者的pH大,A选项错误;
B.V(NaOH)=10.00mL时,氢氧化钠滴定醋酸的溶液中的溶质为等物质的量的CH3COOH和CH3COONa,CH3COOH的电离大于CH3COO-的水解,![]() ,B选项错误;
,B选项错误;
C.醋酸是弱电解质,部分电离,因此恰好中和时,两种酸所用NaOH溶液体积不相等,醋酸用的体积更多,C选项错误;
D.V(NaOH)=20.00mL时,两溶液中的溶质分别是NaCl和CH3COONa,且二者的物质的量相等,考虑CH3COO-水解,故c(Cl-)>c(CH3COO-),D选项正确;
答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,A的单质为密度最小的气体,B、W同周期,A、D同主族,A与W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为______________。写出E的最高价氧化物的水化物与D的最高价氧化物的水化物反应的离子方程式___________________________。
(2)由A、W元素组成的18电子分子的电子式为__________________________。
(3)D的一种氧化物可与B的最高价氧化物反应生成W的单质,试写出反应的化学方程式____________________________。
(4)向含有Fe2+和淀粉KI的溶液中滴入A2W2,观察到溶液呈蓝色并有红褐色沉淀生成。当消耗2mol I- 时,共转移3mol电子,该反应的离子方程式是_______________。
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,DA能与水反应放氢气,若将1mol DA和1mol E单质混合加入足量的水,充分反应后生成气体的体积是_________L(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)广泛应用于有机合成、染料、颜料、催化剂等工业。它是一种白色粉末,微溶于水,不溶于乙醇、稀硝酸及稀硫酸,可溶于氨水、浓盐酸,并生成配合物NH4[CuCl2];能在空气中迅速被氧化成绿色;见光则分解,变成褐色。下图是实验室制备氯化亚铜的流程图及实验装置图。
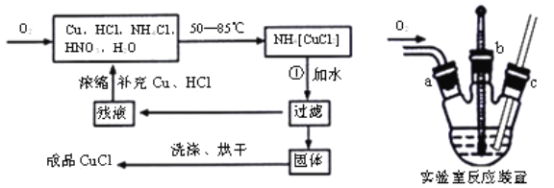
实验药品:铜丝20g、氯化铵20g、65%硝酸l0mL、36%盐酸15mL、水。
(1)请写出①的化学方程式____________________________________。
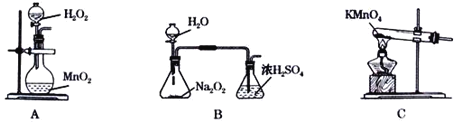
(2)本实验中通入O2的速率不宜过大,宜选择下图中的____(填字母序号)方案,并说明选择该装置的理由__________________________________________。
(3)电炉加热升温至50℃时停止加热,反应快速进行,当烧瓶中液面上方的现象为_____时,停止通入氧气,打开瓶塞,沿C口倾出反应液于l000mL大烧杯中,加水500mL,即刻有大量白色沉淀析出。
(4)关于该实验过程中,下列说法正确的是_________________。
A 实验开始时,温度计显示反应液温度可能低于室温。
B 流程中过滤操作,可以采用真空抽滤的方式,洗涤固体可以用95%的酒精。
C 该实验流程中,残液中补充HCl的主要作用是抑制产物的水解。
D 反应装置中使用长导管的目的是防止三颈烧瓶内气压过大。
(5)氯化亚铜的定量
①称取成品0.25g置于预先放入玻璃珠30粒和l0mL过量的FeCl3溶液的250mL锥形瓶中,不断摇动;
②待样品溶解后,加水50mL,邻菲罗啉指示剂2滴;
③立即用0.l0 mol·L-1硫酸铈标准溶液滴至绿色出现为终点并记录读数,再重复实验二次,测得数据如下表。(已知:CuCl + FeCl3 = CuCl2 + FeCl2 ,Fe2+ + Ce4+ = Fe3+ + Ce3+)
实验序号 | 1 | 2 | 3 |
滴定起始读数(mL) | 0.75 | 0.50 | 0.80 |
滴定终点读数(mL) | 24.70 | 24.95 | 24.85 |
④数据处理:计算得CuCl的纯度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组一定能大量共存的是
A.能使pH试纸显红色的溶液中:Na+、NH4+、I-、NO3-
B.含有0.1mol/L Fe3+的溶液中:K+、Mg2+、S2-、SO32-
C.由水电离出来的c(H+)=1×10-13mol/L的溶液中:K+、CO32-、Cl-、NO3-
D.常温下,![]() 的溶液:Na+、K+、CO32-、NO3-
的溶液:Na+、K+、CO32-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜冶金术以火法治为主,炼铜的副产品SO2多用于制硫酸和石背等化学产品。火法炼铜的工艺流程如下:

反应I:2Cu2S(s)+3O2(g)→2Cu2O(s)+2SO2(g)+768.2kJ
反应II:2Cu2O(s)+Cu2S(s)→6Cu(s)+SO2(g)-116.0kJ
(1)在反应Ⅱ中,每生成1mol SO2转移电子_______mol,反应Cu2S(s)+O2(g)→2Cu(s)+SO2(g)+Q的Q=_____kJ。
(2)理论上m1:m2=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应,X2++Z=X+Z2+,Y+Z2+=Y2++Z。这四种离子被还原成0价时,表现的氧化性强弱顺序为( )
A.R2+>X2+>Z2+>Y2+B.X2+>R2+>Y2+>Z2+
C.Y2+>Z2+>R2+>X2+D.Z2+>X2+>R2+>Y2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸![]() 是一种弱酸,
是一种弱酸,![]() 升华,
升华,![]() 以上分解可放出
以上分解可放出![]() 和CO;可与酸性
和CO;可与酸性![]() 溶液反应;其钠盐易溶于水,钙盐难溶于水。下列说法正确的是
溶液反应;其钠盐易溶于水,钙盐难溶于水。下列说法正确的是![]()
![]()
A.草酸受热产生的气体,用足量的NaOH溶液充分吸收后,可收集得到纯净的CO
B.草酸受热产生的气体通过灼热的氧化铜,若出现黑色变红色现象,则说明产生的气体中一定有CO
C.草酸受热产生的气体直接通入足量的澄清石灰水中,若能产生白色浑浊现象,则说明产生的气体中一定有![]()
D.将![]() 草酸晶体
草酸晶体![]() 加入到
加入到![]() 的NaOH溶液中充分反应,测得反应后溶液呈碱性,其原因是
的NaOH溶液中充分反应,测得反应后溶液呈碱性,其原因是![]() 水解
水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医用酒精和84消毒液混合使用可能发生反应:4NaClO+CH3CH2OH![]() HCCl3+HCOONa+NaCl+2NaOH+H2O,设NA为阿伏加德罗常数,下列叙述正确的是
HCCl3+HCOONa+NaCl+2NaOH+H2O,设NA为阿伏加德罗常数,下列叙述正确的是
A.含NA个ClO-的NaClO溶液中,Na+数目为NA
B.上述反应中,每生成1molNaCl,转移的电子数为8NA
C.100 g质量分数为46%的乙醇溶液中所含的氢原子数为6NA
D.标准状况下,2.24 L HCCl3含有的共用电子对的数目为0.4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com