
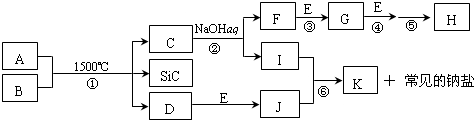
分析 J是一种能引起温室效应的气体,则J为CO2,A、E是空气中的两种主要成分,D是一种单质,D和E反应生成J,则E为O2,D为C,A为N2,B由Si及另外两种元素组成,且Si与另外两种元素的物质的量之比均为1:4,根据元素守恒可知,B为Al4SiC4,C是由两种元素组成的新型材料,且和SiC具有相同的价电子数和原子数,则最外层电子数之和为8,且含有2个原子,应为AlN,与NaOH反应生成F和I,应分别为NH3和NaAlO2,F为气体,则F为NH3,I为NaAlO2,K是两性化合物,K为Al(OH)3,由转化关系可知G为NO,反应③、④、⑤用于工业中生产H,应为氨的催化氧化,工业制硝酸的反应,所以H为HNO3,据此答题.
解答 解:J是一种能引起温室效应的气体,则J为CO2,A、E是空气中的两种主要成分,D是一种单质,D和E反应生成J,则E为O2,D为C,A为N2,B由Si及另外两种元素组成,且Si与另外两种元素的物质的量之比均为1:4,根据元素守恒可知,B为Al4SiC4,C是由两种元素组成的新型材料,且和SiC具有相同的价电子数和原子数,则最外层电子数之和为8,且含有2个原子,应为AlN,与NaOH反应生成F和I,应分别为NH3和NaAlO2,F为气体,则F为NH3,I为NaAlO2,K是两性化合物,K为Al(OH)3,由转化关系可知G为NO,反应③、④、⑤用于工业中生产H,应为氨的催化氧化,工业制硝酸的反应,所以H为HNO3,
(1)由上面的分析可知,F为NH3,I为NaAlO2,
故答案为:NH3;NaAlO2;
(2)反应③为氨气的催化氧化反应,反应的方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(3)反应⑥为二氧化碳与偏铝酸钠的反应,反应的离子方程式为CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-,
故答案为:CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-;
(4)A中含有Al、Si、C等元素,Si与另外两种元素的物质的量之比均为1:4,应为Al4SiC4,与氮气反应生成AlN、SiC和C,
反应的方程式为Al4SiC4+2N2$\frac{\underline{\;1500℃\;}}{\;}$4AlN+SiC+3C,
故答案为:Al4SiC4+2N2$\frac{\underline{\;1500℃\;}}{\;}$4AlN+SiC+3C.
点评 本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力的考查,本题注意以B为解答该题的突破口,把握题给信息,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 ,它的分子式是C10H22
,它的分子式是C10H22查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 最外层电子数比次外层电子数少5个电子 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为:PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )
热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为:PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )| A. | 正极反应式:Ca+2Cl--2e-═CaCl2 | |
| B. | 放电过程中,Li+向负极移动 | |
| C. | 每转移0.1 mol电子,理论上生成20.7 g Pb | |
| D. | 常温时,在正负极间接上电流表或检流计,指针不偏转 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H14 | B. | C7H16 | C. | C8H18 | D. | C9H20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 试剂 | T1/℃ | T2/℃ | T3/℃ |
| NaCO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |
| 温度 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| NaCO3 | 12.5g | 21.5g | 39.7g | 40.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
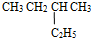 和
和 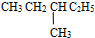 ⑤
⑤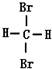 和
和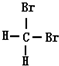
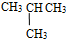 ⑦C2H5OH和C4H9OH
⑦C2H5OH和C4H9OH查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com