
�˹��̵���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̡�
I.���һЩ��ѧ���о����ø����ӵ����Ե�SCY�մɣ��ܴ���H+��ʵ�鵪�Ĺ̶�һ��ⷨ�ϳɰ����������˵�����������ת���ʡ��ܷ�ӦʽΪ��N2(g)��3H2(g)  2NH3(g)�����ڵ�ⷨ�ϳɰ��Ĺ����У�Ӧ��H2���ϵ�ͨ��_________����������������� ������һ�缫ͨ��N2���õ缫�ķ�ӦʽΪ__________________________��
2NH3(g)�����ڵ�ⷨ�ϳɰ��Ĺ����У�Ӧ��H2���ϵ�ͨ��_________����������������� ������һ�缫ͨ��N2���õ缫�ķ�ӦʽΪ__________________________��
II.�ݱ�������һ�������£�N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ����Ҫ����ΪNH3����Ӧ�ķ�Ӧ����ʽΪ��2N2(g)��6H2O(g) 4NH3(g)��3O2(g) ��H��Q��
4NH3(g)��3O2(g) ��H��Q��
��1��������Ӧ��ƽ�ⳣ������ʽΪ_______________��
��2��ȡ��ݵ����N2��H2O�Ļ�����壨���ʵ���֮�Ⱦ�Ϊ1��3�����ֱ���������ͬ�ĺ����ܱ������У����¶Ȳ���ͬ������·�����Ӧ����Ӧ��ͬʱ���õ������������ �뷴Ӧ�¶�T�Ĺ�ϵ������ͼ��ʾ����������Ӧ��Q________0�����������������=������
�뷴Ӧ�¶�T�Ĺ�ϵ������ͼ��ʾ����������Ӧ��Q________0�����������������=������

��3����������Ӧ���д���������·���������ͼ��ʾ��a��b��c��d���������У��ܱ�ʾ��Ӧ��ϵ�����仯����_______��ѡ����ĸ���ţ���ͼ�С�H�ľ���ֵΪ1530kJ��mol-1��

III.Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2(g)��3H2(g)  2NH3(g) ��H����93.0kJ/mol��
2NH3(g) ��H����93.0kJ/mol��
�ش��������⣺
��1�����II�е����ݣ���O2(g)��2H2(g)��2H2O(g)�ġ�H��______________��
��2����һ���¶��£���1molN2��3mol H2����������������ܱ������з�����Ӧ���ﵽƽ��״̬ʱ��������������ʵ���Ϊ2.8mol��
�ٴ�ƽ��ʱ��H2��ת���ʦ�1��______________��
������ͬ�����£�����ʼʱֻ��NH3���ڸ������У��ﵽƽ��״̬ʱNH3��ת����Ϊ��2������1����2��1ʱ������ʼʱNH3�����ʵ���n(NH3)��_____________mol��
��. ����1�֣� N2��6H����6e��===2NH3 ��2�֣�
��.��1��K��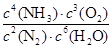 ��2�֣���2������2�֣� ��3��d��2�֣�
��2�֣���2������2�֣� ��3��d��2�֣�
��. ��1����572.0 kJ��mol��1��2�֣���λ��д�����֣� ��2����60%��2�֣� ��2��1�֣�
��������
�����������.����������ʧȥ���ӷ���������Ӧ�������õ����ӣ�������ԭ��Ӧ�����Դ��ܷ�Ӧ�����жϳ�H2�DZ�������Ӧ��������ͨ�룬N2������������ԭ��Ӧ��������ͨ�룬�缫��Ӧʽ��N2+ 6H++6e-��2NH3��
��.��1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ�Ӧ����ʽ��֪���÷�Ӧ��ƽ�ⳣ���ı���ʽK��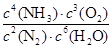 ��
��
��2������������ͬʱ���ڵ���������������¶ȱ仯�Ĺ�ϵ�����ߵı仯��������С���¶����߷�Ӧ���ʼӿ졣�ڴ����У���Ӧ��ͬʱ�䣬�����µ�������δ�ﵽƽ������㣬���¶ȵ����ߣ�����������������¶����߶�������ߵ���ߵ���ij�¶��´ﵽƽ��ĵ㣬֮������㣬����ƽ���ĵ�������������������¶����߶����ͣ���˵�������¶�ƽ��������Ӧ�����ƶ���������ɵ����ķ�Ӧ�Ƿ��ȷ�Ӧ�����˷�Ӧ������ӦΪ���ȷ�Ӧ��
��3�����ݣ�2���Ľ��ۣ���Ӧ�����ȷ�Ӧ��Ӧ��c��d�������Ҵ𰸡�ʹ�ô������Խ��ͷ�Ӧ�Ļ�ܣ����Ӧ��ѡd��
��.��1����Ӧ��N2(g)��3H2(g) 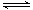 2NH3(g)�ͷ�Ӧ��2N2(g)��6H2O(g)
2NH3(g)�ͷ�Ӧ��2N2(g)��6H2O(g)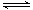 4NH3(g)��3O2(g)����������ݸ�˹���ɿ�֪���١�
4NH3(g)��3O2(g)����������ݸ�˹���ɿ�֪���١�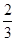 ���ڡ�
���ڡ�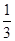 ���õ���ӦO2(g)��2H2(g)��2H2O(g)�����Ը÷�Ӧ�ķ�Ӧ�ȡ�H��2/3������93 kJ��mol��1����1/3��1530
kJ��mol��1����572 kJ��mol��1��
���õ���ӦO2(g)��2H2(g)��2H2O(g)�����Ը÷�Ӧ�ķ�Ӧ�ȡ�H��2/3������93 kJ��mol��1����1/3��1530
kJ��mol��1����572 kJ��mol��1��
��2������N2(g)��3H2(g) 2NH3(g)��֪��4mol�ķ�Ӧ����ȫ��Ӧ�������ʵ�����С2mol����˵����٣�4��2.8��mol��1.2molʱ���μӷ�Ӧ��H2Ϊ1.8mol������������ת����Ϊ
2NH3(g)��֪��4mol�ķ�Ӧ����ȫ��Ӧ�������ʵ�����С2mol����˵����٣�4��2.8��mol��1.2molʱ���μӷ�Ӧ��H2Ϊ1.8mol������������ת����Ϊ ��100%��60����
��100%��60����
���谱�������ʵ�����x����1����2��1�����Ԧ�2��40%��ƽ��ʱ���������ʵ�����1.2mol���������İ�����x��1.2mol����x��40%��x��1.2mol�����x��2.0mol��
���㣺���黯ѧ��Ӧԭ���еĵ绯ѧ����ѧ��Ӧ����ЧӦ����ѧ��Ӧ���ȣ�ƽ��̬�Ľ�����ת���ʡ���ѧƽ���뷴Ӧ�ȵļ��㣩��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ͨ�� |
| һ������ |
| c4(NH3)?c3(O2) |
| c2(N2)?c6(H2O) |
| c4(NH3)?c3(O2) |
| c2(N2)?c6(H2O) |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| 3 |
| 2 |


| 4 |
| 27 |
| 4 |
| 27 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�����ʡ�����ص���ѧ��������ѧ�ȣ�������ѧ������������ѧ�Ծ����������� ���ͣ������
(17��)�˹��̵���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̡��ݱ���,���¡���ѹ������������,N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����Ӧ���Ȼ�ѧ����ʽΪ��N2(g)+3H2O(l) 2NH3(g)+
2NH3(g)+ O2(g) ��H="+765.0kJ" /mol��
O2(g) ��H="+765.0kJ" /mol��
��������ͼ��ʾ�������л���������Ӧ���д�����������������·�Ӧ��ϵ�е������仯ʾ��ͼ�������б�ע(������H)��
��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2(g)+3H2(g) 2NH3(g) ��H=��93.0kJ /mol��
2NH3(g) ��H=��93.0kJ /mol��
�ش��������⣺
(1)������ȼ���ȡ�H=_______________kJ/mol��
(2)�ں��º����ܱ������н��еĺϳɰ���Ӧ�������ܱ�ʾ�ﵽƽ��״̬����_______(�����)��
a����������ѹǿ���ٷ����仯
b�����������ܶȲ��ٷ����仯
c����Ӧ������N2��NH3�����ʵ����ı�ֵ���ٷ����仯
d����λʱ���ڶϿ�a��H��H����ͬʱ�γ�3 a��N��H��
e���������ʵ�Ũ�ȱ�ǡ�õ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮��
(3)�ں��º��ݵ��ܱ������У��ϳɰ���Ӧ�ĸ�����Ũ�ȱ仯��������ͼ��ʾ����ش��������⣺
�� ��ʾN2��Ũ�ȱ仯�������� (ѡ�����ߴ��š�A������B����C��)��
�� ǰ25 min �ڣ���H2��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧƽ�������� ��
����25 min ĩ��Ӧ�պôﵽƽ�⣬����¶��·�Ӧ��ƽ�ⳣ��K = (���������÷�����ʾ)���������¶ȣ��÷�Ӧ��ƽ�ⳣ��ֵ��_______(���������С�����䡱)��
(4)�ڵ�25 min ĩ�����������������䣬�����߷�Ӧ�¶Ȳ��跨���ָ��¶Ȳ��䣬�ڵ�35 minĩ�ٴδﵽƽ�⡣ƽ���ƶ�������H2Ũ�ȱ仯��1.5 mol��L��1��������ͼ�л�����25 min �� 40 min NH3Ũ�ȱ仯���ߡ�
(5)��һ���¶��£���1 mol N2��3 mol H2����������������ܱ������з�����Ӧ���ﵽƽ��״̬ʱ��������������ʵ���Ϊ2.8 mol ��
�ٴ�ƽ��ʱ��H2��ת������1 = ____________��
������ͬ�����£�����ʼʱֻ��NH3���ڸ������У��ﵽƽ��״̬ʱNH3��ת����Ϊ��2������1 + ��2 =1ʱ������ʼʱn (NH3)= ________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��ɽ��ʡ�ij��и�����ѧ���ڳ����Ի�ѧ�Ծ��������棩 ���ͣ������
�˹��̵���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̡��ݱ���,���¡���ѹ������������,N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����Ӧ���Ȼ�ѧ����ʽΪ��N2(g)+3H2O(l) 2NH3(g)+
2NH3(g)+ O2(g) ��H="+765.0kJ" /mol��
O2(g) ��H="+765.0kJ" /mol��
��������ͼ��ʾ�������л���������Ӧ���д�����������������·�Ӧ��ϵ�е������仯ʾ��ͼ�������б�ע(������H)��

��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2(g)+
3H2(g) 2NH3(g) ��H=��93.0kJ /mol��
2NH3(g) ��H=��93.0kJ /mol��
�ش��������⣺
(1)������ȼ���ȡ�H=_______________kJ/mol��
(2)�ں��º����ܱ������н��еĺϳɰ���Ӧ�������ܱ�ʾ�ﵽƽ��״̬����_______(�����)��
a����������ѹǿ���ٷ����仯
b�����������ܶȲ��ٷ����仯
c����Ӧ������N2��NH3�����ʵ����ı�ֵ���ٷ����仯
d����λʱ���ڶϿ�a��H��H����ͬʱ�γ�3 a��N��H��
e���������ʵ�Ũ�ȱ�ǡ�õ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮��
(3)�ں��º��ݵ��ܱ������У��ϳɰ���Ӧ�ĸ�����Ũ�ȱ仯��������ͼ��ʾ����ش��������⣺
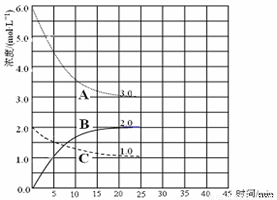
�� ��ʾN2��Ũ�ȱ仯�������� (ѡ�����ߴ��š�A������B����C��)��
�� ǰ25 min �ڣ���H2��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧƽ�������� ��
����25 min ĩ��Ӧ�պôﵽƽ�⣬����¶��·�Ӧ��ƽ�ⳣ��K = (���������÷�����ʾ)���������¶ȣ��÷�Ӧ��ƽ�ⳣ��ֵ��_______(����� ����С�����䡱)��
(4)�ڵ�25 min ĩ�����������������䣬�����߷�Ӧ�¶Ȳ��跨���ָ��¶Ȳ��䣬�ڵ�35 minĩ�ٴδﵽƽ�⡣ƽ���ƶ�������H2Ũ�ȱ仯��1.5 mol��L��1��������ͼ�л�����25 min �� 40 min NH3Ũ�ȱ仯���ߡ�
(5)��һ���¶��£���1 mol N2��3 mol H2����������������ܱ������з�����Ӧ���ﵽƽ��״̬ʱ��������������ʵ���Ϊ2.8 mol ��
�ٴ�ƽ��ʱ��H2��ת���ʦ�1 = ____________��
������ͬ�����£�����ʼʱֻ��NH3���ڸ������У��ﵽƽ��״̬ʱNH3��ת����Ϊ��2������1 + ��2 =1ʱ������ʼʱn (NH3)= ________mol��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com