
【题目】碱金属和卤素形成的化合物大多数具有的性质是( )
①高沸点 ②能溶于水 ③水溶液能导电 ④低熔点 ⑤熔融状态不导电
A.①④⑤B.①②③C.②③⑤D.③④⑤
科目:高中化学 来源: 题型:
【题目】为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请完成下列问题.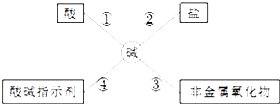
(1)氢氧化钠具有强烈的 , 使用时必须十分小心,实验时最好戴防护眼镜.
(2)为了验证④,小丽将紫色石蕊溶液分别滴入氢氧化钠溶液和澄清石灰水中,溶液变成蓝色,原因是它们在水溶液中能电离出 .
(3)依据反应③什么氢氧化钠必须密封保存否则在空气中要变质;反应的化学方程式为 . 要检验该氢氧化钠溶液已变质,可以选用的试剂是 . (写出化学式)
(4)依据反应②,氢氧化钙溶液能与下列物质反应的是(填序号).
A.稀硫酸
B.氯化钠溶液
C.硫酸铜溶液
D.碳酸钠溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论正确的是
 A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
B.容器中发生的反应可表示为3X(g)+Y(g) ![]() 2Z(g)
2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】漂白粉是用Cl2与_______反应来制取的,漂白粉是________填“混合物”或“纯净物”),其有效成分为_______(以上均填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L
B.从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol/L
C.配制480 mL 0.5 mol/L的CuSO4溶液,需62.5 g胆矾
D.10 g 98%的硫酸(密度为1.84 gcm﹣3)与10 mL18.4 molL﹣1的硫酸的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅及其化合物用途非常广泛,已知铅(Pb)与硅同主族且Pb比Si多3个电子层。回答下列问题:
(1)铅位于元素周期表的第__________周期__________族。
(2)难溶物PbSO4溶于CH3COONH4溶液可制得(CH3COO)2Pb [(CH3COO)2Pb易溶于水],发生的反应为 PbSO4+2CH3COONH4=(CH3COO)2Pb +(NH4)2SO4,说明(CH3COO)2Pb是_______(填“强”或“弱”)电解质。
(3)铅蓄电池充放电原理为Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,其中工作“B”为________(填“放电”或“充电”);电解质不能用浓盐酸,否则电池失效并放出大量的氯气,其原因是________(用化学方程式表示)。
2PbSO4+2H2O,其中工作“B”为________(填“放电”或“充电”);电解质不能用浓盐酸,否则电池失效并放出大量的氯气,其原因是________(用化学方程式表示)。
(4)将PbO2加入硝酸酸化的Mn(NO3)2溶液中,揽拌后溶液显紫红色。则每反应1 molMn(NO3)2,转移______________mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学实验中必须注意安全,以下实验操作或事故处理正确的是( )
①在点燃H2 , CO,CH4等易燃气体前,必须检验气体的纯度
②在稀释浓硫酸时,应将浓硫酸沿器壁慢慢注入水中并不断用玻璃棒搅拌
③浓碱液对皮肤有腐蚀性,如果不慎沾到皮肤上,应用较多的水冲洗,再涂上硼酸溶液
④给试管中的液体加热时,液体体积应不超过试管容积的三分之一
⑤点燃添满酒精的酒精灯
⑥给试管中的液体加热时,试管口不能对着自己或他人.
A.⑤⑥
B.①②③
C.①②③④⑥
D.全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com