
分析 根据n=$\frac{V}{Vm}$计算HCl的物质的量,根据m=nM计算HCl的质量,根据m=ρV计算水的质量,进而计算溶液质量,再根据V=$\frac{m}{ρ}$计算溶液体积,根据c=$\frac{n}{V}$计算溶液物质的量浓度,根据$\frac{溶质质量}{溶液质量}$×100%计算溶液质量分数.
解答 解:设烧瓶的体积为VL,则HCl的体积为1L,其物质的量为$\frac{1}{22.4}$mol,则HCl的质量为$\frac{36.5}{22.4}$g,1L水的质量为1000g,故溶液质量为1000g+$\frac{36.5}{22.4}$g,
则溶液体积为:$\frac{1000g+\frac{36.5}{22.4}g}{ρg•c{m}^{-3}}$mL=$\frac{22400+36.5}{22.4ρ}$mL=$\frac{22.4+0.0365}{22.4ρ}$L,
故溶液物质的量浓度为:c=$\frac{n}{V}$=$\frac{\frac{1}{22.4}mol}{\frac{22.4+0.0365}{22.4ρ}L}$=$\frac{ρ}{22.4+0.0365}$mol/L,
溶液质量分数为$\frac{溶质质量}{溶液质量}$×100%=$\frac{\frac{36.5}{22.4}g}{1000g+\frac{36.5}{22.4}g}$×100%=$\frac{36.5}{22436.5}$×100%=0.163%,
故答案为:$\frac{ρ}{22.4+0.0365}$mol/L;0.163%.
点评 本题考查溶液浓度计算,涉及物质的量浓度、质量分数计算,注意对公式的理解,题目计算量较大,为易错题目.


 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:解答题
 《Nature》报道了我国科学家通过测量化石中26AI和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”.回答下列问题:
《Nature》报道了我国科学家通过测量化石中26AI和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”.回答下列问题:| 仪器代号 | 所装试剂 | 装置作用 |
| A | 石灰石和1mol/L硝酸. | 制取CO2证明硝酸比碳酸强 |
| C | 饱和碳酸氢钠溶液 | 除去CO2中的硝酸蒸气 |
| C | 硅酸钠溶液 | 证明碳酸强于硅酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH<7的溶液中:K+、Fe2+、SO42-、NO3- | |
| B. | 无色透明溶液中:Ca2+、Cu2+、ClO-、Cl- | |
| C. | NaAlO2溶液中:Al3+、Fe3+、NO3-、CH3COO- | |
| D. | 由水电离出的c(H+)=10-12mol•L-1的溶液中:Mg2+、Cu2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应阶段 | Ⅰ | Ⅱ | Ⅲ |
| 稀盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现 象 | 无气体 | 有气体 | 无气体 |
| A. | 1.00mol•L-1 | B. | 0.50mol•L-1 | C. | 1.50mol•L-1 | D. | 2.00mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
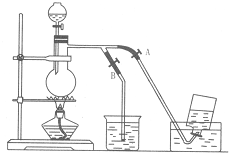 如图表示在没有通风橱收纯净的氯气时设计的装置,图中A、B是可控制的弹簧铁夹.
如图表示在没有通风橱收纯净的氯气时设计的装置,图中A、B是可控制的弹簧铁夹. 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com