
| A. | 一定存在Fe2+、Na+、Cl- | B. | 一定不存在I-、SO32- | ||
| C. | 一定呈碱性 | D. | 一定存在NH4+ |
分析 将该溶液加少量新制氯水,溶液变黄色,溶液中可能存在Fe2+、I-,再向上述反应后溶液中加入BaCl2溶液或淀粉溶液,均无明显现象,则说明溶液中不存在SO32-、I-,则一定存在Fe2+;根据离子共存可知,溶液中一定不存在CO32-;结合溶液电中性可知,溶液中一定存在Cl-,可能存在Na+、NH4+,据此进行解答.
解答 解:将该溶液加少量新制氯水,溶液变黄色,溶液中可能存在Fe2+、I-,再向上述反应后溶液中加入BaCl2溶液或淀粉溶液,均无明显现象,则说明溶液中不存在SO32-、I-,则一定存在Fe2+;根据离子共存可知,溶液中一定不存在CO32-;结合溶液电中性可知,溶液中一定存在Cl-,可能存在Na+、NH4+,
根据分析可知,溶液中一定存在的离子为:Fe2+、Cl-,一定不存在的离子为:I-、CO32-、SO32-,可能存在Na+、NH4+,
A.溶液中一定存在Fe2+、Cl-,无法确定是否存在Na+,故A错误;
B.溶液中一定不存在一定不存在I-、SO32-,故B正确;
C.溶液中存在亚铁离子,亚铁离子水解,溶液显示酸性,故C错误;
D.溶液中不一定存在铵根离子,故D错误;
故选B.
点评 本题考查了常见离子的检验,题目难度中等,明确常见离子的性质及检验方法为解答关键,试题侧重考查显示的分析、理解能力,根据电中性判断氯离子的存在情况为易错点.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:解答题
 .
.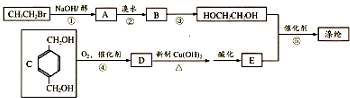
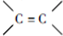 ,反应①、②的反应类型分别为消去反应、加成反应,有机物B的名称是1,2-二溴乙烷,反应③可用的试剂为氢氧化钠水溶液;
,反应①、②的反应类型分别为消去反应、加成反应,有机物B的名称是1,2-二溴乙烷,反应③可用的试剂为氢氧化钠水溶液;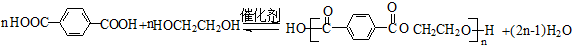 ;
;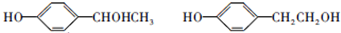 ;
;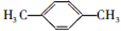 ;F的一种同系物G比F多2个碳原子,其中苯环上只有一个取代基的G的结构有4种.
;F的一种同系物G比F多2个碳原子,其中苯环上只有一个取代基的G的结构有4种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 产物Cu2HgI4中,Cu元素的化合价为+2 | |
| B. | 由Cu2+与I-直接反应制得CuI的离子方程式为Cu2++I-=CuI | |
| C. | 该反应的氧化剂CuI,氧化产物为Cu | |
| D. | 当有2molCuI参与反应时,转移电子为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
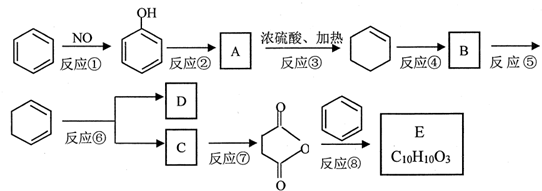
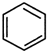 +(CH3CO)2O→
+(CH3CO)2O→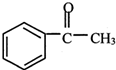 +CH3COOH
+CH3COOH ; B
; B
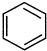 直接制取
直接制取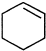 ,原因是苯中的碳碳键是一种特殊的键,与氢气加成后只能得环已烷.
,原因是苯中的碳碳键是一种特殊的键,与氢气加成后只能得环已烷.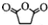 +
+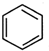 →
→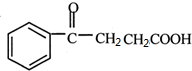 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子与原子之间 | B. | 分子与分子之间 | C. | 离子与离子之间 | D. | 离子与电子之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | A | B | C | D |
| n(H2SO4)/mol | 2 | 3 | 4 | 5 |
| n(沉淀)/mol | 2 | 3 | 2 | 1.5 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 也可发生类似反应①的反应,生成化合物Ⅳ:
也可发生类似反应①的反应,生成化合物Ⅳ: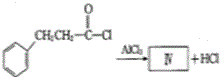
 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com