
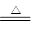
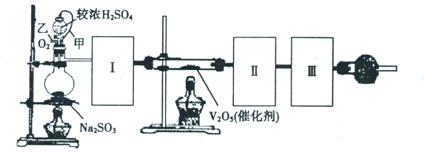
 2SO3(略反应条件和可逆号)(2分,反应条件和可逆号各占1分)
2SO3(略反应条件和可逆号)(2分,反应条件和可逆号各占1分)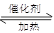 2SO3。
2SO3。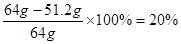 。
。

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源:不详 题型:单选题
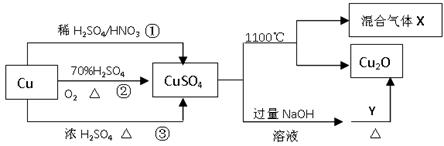
| A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3∶2 |
| B.相对于途径①、③,途径②更好地体现了绿色化学思想 |
| C.1molCuSO4在1100℃所得混合气体X中O2一定为0.75mol |
| D.Y可以是葡萄糖 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
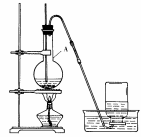
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③④⑤⑥⑦⑧ | B.②③⑤⑥⑦⑧⑨ |
| C.①②③⑤⑥⑦⑨ | D.①②③④⑤⑥⑨ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
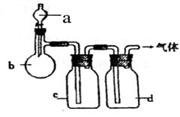
| 选项 | 气体 | a | b | c | d |
| A | CO2 | 盐酸 | CaCO3 | 饱和Na2CO3溶液 | 浓硫酸 |
| B | Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓硫酸 |
| C | NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 固体NaOH |
| D | NO | 稀硝酸 | 铜屑 | H2O | 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
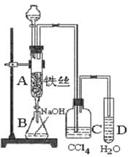
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
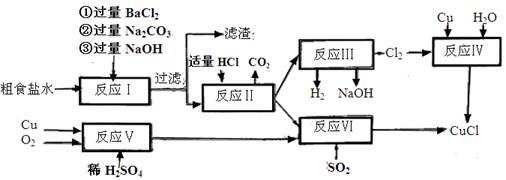
 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。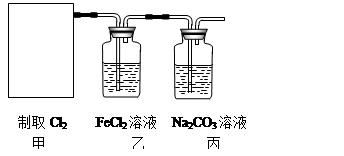
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

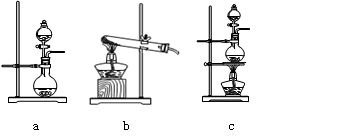
| 分项 内容 | CO2发生装置(X) 随开随用,随关随停 | 除杂洗气装置(Y) | 制备产品装置(Z) |
| 选择的装置(填序号) | | | C |
| 选择的药品(填序号) | | | ① |
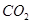 发生装置(X)的气密性,请写出主要操作过程:
发生装置(X)的气密性,请写出主要操作过程: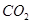 气体,其原因是_________________;通入过量
气体,其原因是_________________;通入过量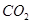 后,Z装置内的溶液中离子浓度大小顺序为:_______________________ 。
后,Z装置内的溶液中离子浓度大小顺序为:_______________________ 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com