
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤 正确的操作顺序( )
A.①②③⑤④ B.③②①⑤④ C.②③①④⑤ D.③⑤②①④
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案科目:高中化学 来源: 题型:
氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:
H2 (g) + 1/2O2(g) == H2O (l); △H = -285.8 KJ/mol
CO(g) + 1/2O2(g) == CO2(g); △H = -283.0 KJ/mol
C8H18 (l) +(25/2)O2(g) == 8CO2(g) + 9H2O (l); △H = -5518 KJ/mol
CH4 (g) + 2O2(g) == CO2(g) + 2H2O  (l); △H = -890.3 KJ/mol
(l); △H = -890.3 KJ/mol
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是
A.H2 (g) B.CO(g)
C.C8H18 (l) D.CH4 (g)
查看答案和解析>>
科目:高中化学 来源: 题型:
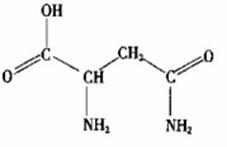
芦笋中的天冬酰胺(结构如下图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。
(1)天冬酰胺所含元素中,____ 元素基态原子核外未成对电子数最多; 元素第一电离能最大。
(2)H2S和H2Se的参数对比见右表。
①H2Se的晶体类型为_________,含有的共价键类型为_________。
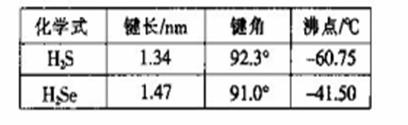
 ②H2S的键角大于H2Se的原因可能为____________________ 。
②H2S的键角大于H2Se的原因可能为____________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中存在多种平衡,请根据所学化学知识回答下列问题:
(1)在浓度均为0.1mol/L①CH3COONH4 ②NH4HSO4 ③NH3.H2O ④(NH4)2SO4溶液中,NH4+浓度由大到小的顺序为 (填序号)
(2)浓度均为0.1 mol·L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号) 。
(3)恒温下,向pH=6的蒸馏水中加入2.3g金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是 ( )
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶转移液体
A.①和② B.①和③ C.③和④ D.①和④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于 0.2 mol/L 硝酸钾溶液的叙述中,正确的是 ( )
A.1 L 该溶液中含硝酸钾 202 g
B.100 mL 该溶液中含硝酸钾 0.02 mol
C.从 1 L 该溶液中取出 500 mL 后,剩余溶液的浓度为 0.1 mol/L
D.1 L 水中溶解 0.2 mol 硝酸钾,即可配得 0.2 mol/L 硝酸钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在溶液中一定能大量共存的是
A.1.0mol/L的KNO3溶液:H+、Fe2+、Cl一、SO42一
B.与铝反应产生大量氢气的溶液:Na+、K+、HCO3—、NO3一
C. pH=12的溶液: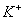 、
、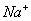 、
、 、Br-
、Br-
D. 由水电离产生的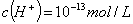 的溶液:
的溶液: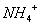 、
、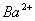 、
、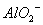 、
、
查看答案和解析>>
科目:高中化学 来源: 题型:
研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究。填写下列空白。
【方案一】将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。
实验中发生反应的化学方程式是
〖实验步骤〗
(1)称取5.4 g铝镁合金粉末样品,溶于V mL 2.0 mol/L NaOH溶液中,充分反应。则NaOH溶液的体积V ≥
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将
(填“偏高”、“偏低”或“无影响”)。
 【方案二】将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况
【方案二】将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况
(约20℃,1.01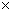 105Pa)的体积。
105Pa)的体积。
〖问题讨论〗
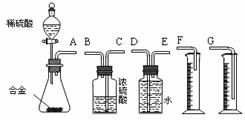
(1)同学们拟选用下列实验装置完成实验:
①你认为最简易的装置其连接顺序是:A接( )( )接( )( )接( )(填接口字母,可不填满。)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,发现稀硫酸不能顺利滴入锥形瓶。请你帮助分析原因
③实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
 D.视线与凹液面最低点水平,读取量筒中水的体积
D.视线与凹液面最低点水平,读取量筒中水的体积
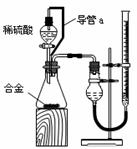
(2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了右图所示的实验装置。
①装置中导管a的作用有:使分液漏斗内气体压强与锥形瓶内气体压强相等,打开分液漏斗活塞时稀硫酸能顺利滴下和
②实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL。则产生氢气的体积为_____ mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com