
【题目】下列指定反应的离子方程式正确的是( )
A.SO2与过量氨水反应:SO2+NH3·H2O=NH4++HSO3-
B.FeCl3溶液与SnCl2溶液反应:Fe3++Sn2+=Fe2++Sn4+
C.Cu与稀硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
D.用浓盐酸与MnO2制取少量Cl2:MnO2+4H++4Cl-![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列卤代烃在KOH醇溶液中加热不反应的是( )
①![]() ;②
;②![]() ;③(CH3)3C–CHBr2;④CHCl2–CHBr2;⑤
;③(CH3)3C–CHBr2;④CHCl2–CHBr2;⑤![]() ;⑥CH3Cl
;⑥CH3Cl
A.全部B.②④C.①③⑥D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)室温下,pH=3的CH3COOH溶液加水稀释到原体积的10倍,溶液的pH值范围_____;
(2)室温下,pH=1和pH=3的硫酸等体积混合后溶液的pH=_____(lg2=0.3、lg3=0.477、lg5=0.7)
(3)在25℃时,100ml 0.6mol/L的盐酸与等体积0.4mol/L的氢氧化钠溶液混合后,溶液pH=______
Ⅱ.某烧碱样品含少量不与酸作用的杂质,为了测定其纯度,进行以下滴定操作:
A.在250 mL的容量瓶中定容配成250 mL烧碱溶液
B.用移液管移取25 mL烧碱溶液于锥形瓶中并滴几滴指示剂甲基橙
C.在天平上准确称取烧碱样品Wg,在烧杯中用蒸馏水溶解
D.将物质的量浓度为c的标准盐酸溶液装入酸式滴定管调节液面,记下开始读数为V1
E.在锥形瓶下垫一张白纸,滴定至终点,记下读数V2
回答下列各问题:
(1)正确操作步骤的顺序是(用字母填写)_____→_____→_____→D→_____。
(2)D步骤中尖嘴部分应_____________________。
(3)滴定终点时锥形瓶中颜色变化____________。
(4)若酸式滴定管不用标准盐酸润洗,在其他操作均正确的前提下,会对测定结果(指烧碱的纯度)有何影响?_____(填“偏高”、“偏低”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用铝热炼镁还原渣[Al、Ca(AlO2)2、Al2O3、MgO及少量不能被碱液溶出的尖晶石型铝的化合物等]制取Al(OH)3的工艺流程如下:
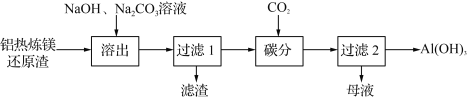
(1) “滤渣”成分包括:水合铝酸钙、尖晶石型铝的化合物、不含铝的化合物______________(写两种物质的化学式)。
(2) “溶出”时,在适当条件下,铝及其大部分含铝化合物以NaAlO2溶出。
①金属Al与NaOH溶液反应的化学方程式为________________________________。
②其他条件相同时,Na2CO3、NaOH溶液的浓度对铝的溶出率的影响如图所示:
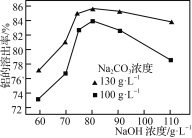
NaOH溶液浓度一定时,130 g·L-1的Na2CO3溶液对铝的溶出率比100 g·L-1的大,这是因为______________(从平衡移动角度分析);Na2CO3溶液浓度一定时,当NaOH溶液浓度大于80 g·L-1,铝的溶出率随NaOH溶液浓度增大而减小,可能原因是______________。
(3) “碳分”时,溶液与过量CO2反应的离子方程式为________________________。
(4) “过滤2”的母液经再生处理可返回“溶出”工序循环使用,再生的方法是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是由常见元素组成的一些单质及其化合物之间的转化关系图。各方框表示有关的一种反应物或生成物(部分物质已经略去)。其中A、B、D在常温下均为无色无味的气体,C是能使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。

(1)写出C→E的化学方程式: 。
(2)实验室常用加热两种固体混合物的方法制备物质C,其化学方程式为: ,干燥C常用 (填写试剂名称)。
(3)E物质遇到D物质时,会观察到 现象,若用排水法收集F,则最终集气瓶中收集到的气体为 (填写物质的化学式)。
(4)写出A→D的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按照课本实验要求,用 50mL 0.50 mol·L-1 的盐酸与 50mL 0.50 mol·L-1 的NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量计算反应热。下列 说法中,不正确的是( )
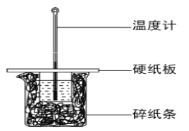
A.实验过程中有一定的热量损失
B.图中实验装置缺少环形玻璃搅拌棒
C.烧杯间填满碎纸条的主要作用是固定小烧杯
D.若将盐酸体积改为 60 mL,理论上所求反应热相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关化学反应原理的说法正确的是( )
A.对任何化学反应来说,反应速率越大,反应现象就越明显
B.反应物的热效应与是否使用催化剂无关
C.已知中和热![]()
![]() ,则1mol浓
,则1mol浓![]() 和1mol
和1mol![]() 的反应热
的反应热![]()
D.向![]() 溶液中通入少量HCl气体,溶液的导电性明显增强
溶液中通入少量HCl气体,溶液的导电性明显增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒酚是植物挥发油的成分之一,它的结构简式为: ![]() ,请回答:
,请回答:
(1)胡椒酚所含官能团的名称为____。
(2)它能发生的化学反应是___(填序号)。
①氧化反应 ② 取代反应 ③ 加成反应 ④消去反应 ⑤ 加聚反应
(3)1 mol 胡椒酚与氢气发生加成反应,理论上最多消耗____ mol H2。
(4)1 mol 胡椒酚与浓溴水发生反应,理论上最多消耗_____mol Br2。
(5)若要制备胡椒酚钠,可以选择的试剂是____(填序号)。
① Na ② NaOH ③ NaHCO3 ④ Na2CO3
(6)写出所有符合下列条件的胡椒酚的同分异构体的结构简式:____。
① 能发生银镜反应;② 苯环上有两个取代基,且苯环上的一氯代物有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烷烃和某气态单烯烃(只含一个碳碳双键)组成的混合气体在同温、同压下是氢气密度的13倍,取标准状况下此混合气体4.48L,通入足量溴水中,溴水质量增加2.8g,则此混合气体可能是( )
A.甲烷和丙烯B.乙烷和丙烯
C.甲烷和2-甲基丙烯D.乙烷和1-丁烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com