BC
分析:A.气体摩尔体积v
m=22.4L/mol的使用条件是标准状况(0℃、101kPa);
B.将质量换算物质的量,结合分子中的质子数进行计算;
C.1个铝原子失去3个电子形成铝离子,根据n=

,计算铝的物质的量,再根据N=nN
A计算失去电子数;
D.根据n=cV=

计算;
解答:A.在常温常压下,不是标准状况,不能使用气体摩尔体积v
m=22.4L/mol,故A错误;
B.2.8gCO物质的量为n=

=
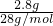
=0.1mol,1molCO中含质子为14mol,所以0.1molCO含质子数为1.4N
A,故B正确;
C.2.7g金属铝变成铝离子时失去的电子数目为
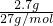
×3×N
Amol
-1=0.3N
A,故C正确;
D.n(K
2SO
4)=2L×0.1mol/L=0.2mol,N(K
+)=0.2mol×2×N
A/mol=0.4N
A,N(SO
42-)=0.2mol×1×N
A/mol=0.2N
A,所以离子总数约为0.6 N
A故D错误;
故选BC.
点评:本题考查了阿伏伽德罗常数的应用,注意阿伏伽德罗常数与气体摩尔体积、物质的量浓度的使用范围和条件,难度不大.

 ,计算铝的物质的量,再根据N=nNA计算失去电子数;
,计算铝的物质的量,再根据N=nNA计算失去电子数; 计算;
计算; =
=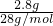 =0.1mol,1molCO中含质子为14mol,所以0.1molCO含质子数为1.4NA,故B正确;
=0.1mol,1molCO中含质子为14mol,所以0.1molCO含质子数为1.4NA,故B正确;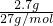 ×3×NAmol-1=0.3NA,故C正确;
×3×NAmol-1=0.3NA,故C正确;
