
实验室用如图的仪器药品制取氯化铁粉末,已知信息:氯化铁粉末易吸水生成结晶水化合物FeCl3+6H2O=FeCl3•6H2O。
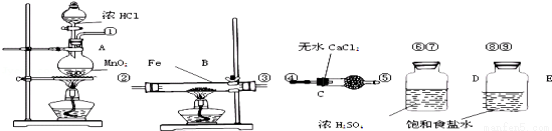
(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序)
接 , 接 , 接 , 接 ;
烧瓶A中反应的离子方程式是 ;
(2)仪器C名称 ,安装它的实验目的是 ,容器E作用是 ;
(3)A、B中的酒精灯应先点燃 处(填“A”或“B”)酒精灯,反应一段时间,再点燃另一个。理由是 ;
(4)这套实验装置是否完整? (填“是”或“否”),若不完整还须补充 装置(若第一问填“是”,则此问不需作答).
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源:2015-2016学年福建三明一中高一上学期第二次月考化学卷(解析版) 题型:选择题
现有四种溶液:①NH4Cl,②(NH4)2SO4,③NaCl,④Na2SO4,下列试剂能将它们区别开的是
A.HCl B.BaCl2 C.NaOH D.Ba(OH)2
查看答案和解析>>
科目:高中化学 来源:2016届云南师大附属中学高三上适应性月考理综化学试卷(解析版) 题型:填空题
硫及其化合物有广泛应用。
(l)硫酸生产过程中涉及以下反应。已知25℃、10lkPa时:
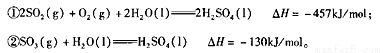
则SO2催化氧化为SO3(g)的热化学方程式为
(2)对于SO2催化氧化为SO3的反应。
①图甲是SO2(g)和SO3(g)的浓度随时间t的变化情况。反应从开始到达到平衡时,用O2表示的平均反应速率为
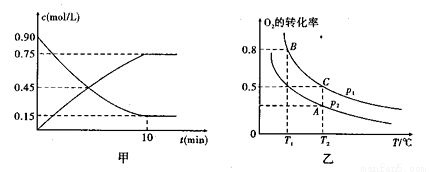
②在一容积可变的密闭容器中充入20mol SO2(g)和10mol O2(g),O2的平衡转化率随温度(T)、压强(p)的变化如图乙所示。则p1与p2的大小关系是p1 p2:(填“>”“<”或“=”);A、B、C三点的平衡常数大小关系为 (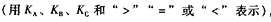 ),理由是
),理由是
(3)工业生产硫酸过程中,通常用氨水吸收尾气
①如果在25℃时,相同物质的量的SO2与NH3溶于水,发生反应的离子方程式为
所得溶液中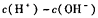 = (填序号)。
= (填序号)。
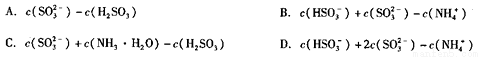
②已知在25℃时NH3·H2O、H2SO3电离平衡常数如下表,则上述所得溶液中,各离子浓度由大到小的顺序为

查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁实验中学分校高二上12月月考化学卷(解析版) 题型:填空题
下图为苯和溴的取代反应的改进实验装置图。其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入铁屑粉少量。
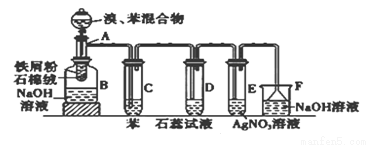
填写下列空白:(注:溴苯与NaOH溶液不可以发生水解反应)
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所有反应的化学方程式___________________________。
(2)试管C中苯的作用是________________;反应开始后,观察D和E试管,看到的现象为D中___________;E中 ;
(3)在上述整套装置中,具有防倒吸的仪器有___________________(填字母)
(4)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这3个优点外,还有一个优点是_______________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上12月月考化学试卷(解析版) 题型:选择题
已知298K时,Mg(OH)2的溶度积常数KSP=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13.0,则下列说法不正确的是
A.所得溶液中的c(H+)=10-13 mol/L
B.所加烧碱溶液的pH=13.0
C.所得溶液中由水电离出的c(OH-)=10-13 mol/L
D.所得溶液中的c(Mg2+)=5.6×10-10 mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一上12月月考化学试卷(解析版) 题型:选择题
向下列溶液中通过量的CO2,一定产生浑浊的是
A、澄清石灰水 B、BaCl2溶液 C、NaAlO2溶液 D、Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二上期中测试化学试卷(解析版) 题型:填空题
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁
已知:
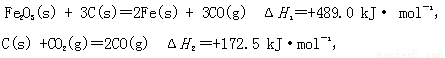
则CO 还原Fe2O3(s)的热化学方程式为 。
(2)尾气中的CO 主要来自于汽油不完全燃烧。有人设想按下列反应除去CO:
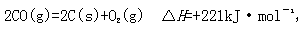 ,简述该设想能否实现的依据: 。
,简述该设想能否实现的依据: 。
(3)CO2 和H2 充入一定体积的密闭容器中,在两种温度下发生反应: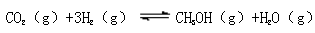
测得CH3OH 的物质的量随时间的变化如图所示。

①曲线I、Ⅱ对应的平衡常数大小关系为KⅠ KⅡ(填“>”或“=”或“<”)。
②一定温度下,此反应在恒.压.容器中进行,能判断该反应达到化学平衡状态的依据是 。
a.容器中压强不变b.H2 的体积分数不变
c.c(H2)=3c(CH3OH) d.容器中密度不变
e.2 个C=O 断裂的同时有6 个H-H 断裂
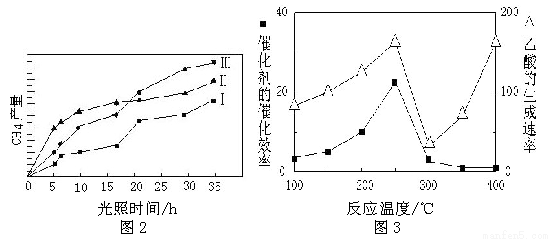
(4)利用光能和光催化剂,可将CO2 和H2O(g)转化为CH4 和O2。紫外光照射时,在不同催化剂(I、II、III)作用下,CH4 产量随光照时间的变化如下图2。在0~15 小时内,CH4 的平均生成速率I、II 和III 从小到大的顺序为 (填序号)。
(5)以TiO2/Cu2Al2O4 为催化剂,可以将CO2 和CH4 直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如下图3:
①当温度在 范围时,温度是乙酸生成速率的主要影响因素。
②Cu2Al2O4难溶于水,可溶于浓硝酸并放出红棕色气体,写出反应的离子方程 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西省钦南区高一上学期期中质量调研化学试卷(解析版) 题型:选择题
在热的稀硫酸溶液中溶解了11.4g FeSO4,当加入50mL 0.5mol·L-1KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3溶液也完全反应,并有NxOy气体逸出,则该NxOy是
A.N2O B.NO C.N2O3 D.NO2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:选择题
工业生产水煤气的反应为:C(s)+H2O(g)  CO(g)+H2(g) ΔH=+131.4kJ·mol-1 下列判断正确的是
CO(g)+H2(g) ΔH=+131.4kJ·mol-1 下列判断正确的是
A.水煤气反应中,生成1molH2(g)吸收131.4 kJ热量
B.CO(g)+H2(g)  C(s)+H2O(g) ΔH=+131.4kJ·mol-1
C(s)+H2O(g) ΔH=+131.4kJ·mol-1
C.水煤气反应中生成1体积CO(g)吸收131.4 kJ热量
D.反应物能量总和大于生成物能量总和
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com