
【题目】碳化硅的结构类似于金刚石的晶体,其中碳原子和硅原子的位置是交替的。在下列三种晶体①金刚石 ②晶体硅 ③碳化硅中,它们的熔点从高到低的顺序是
A.①③② B.②③① C.③①② D.②①③
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. MgCO3![]() MgCl2(aq)
MgCl2(aq)![]() Mg
Mg
B. NaCl(aq)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
C. Cu2(OH)2CO3![]() CuO
CuO![]() Cu(OH)2
Cu(OH)2
D. SO2![]() NH4HSO3
NH4HSO3![]() (NH4)2SO4
(NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】湿法炼锌产生的铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。一种由铜镉渣生产金属镉的流程如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol/L计算):
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 |
沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(1)浸出过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出,其离子方程式是__________________。
(2)除钴过程中,锌粉会与As2O3形成微电池产生AsH3。该微电池的正极反应式为_____。
(3)除铁时先加入适量KMnO4,再加入ZnO调节pH。
① 除铁过程中,理论上参加反应的物质n(KMnO4)∶n(Fe2+)=_________。
② 除铁时加入ZnO控制反应液pH的范围为________________。
(4)若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证:_____________________。
(5)净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷石膏是湿法生产磷酸排出的工业废渣,主要成分是CaSO4·2H2O。
⑴CaSO4·2H2O脱水反应相关的热化学方程式为:
CaSO4·2H2O(s)=CaSO4·![]() H2O(s)+
H2O(s)+![]() H2O(g) ΔH1=83.2 kJ·mol-1
H2O(g) ΔH1=83.2 kJ·mol-1
CaSO4·2H2O(s)=CaSO4(s)+2H2O(l) ΔH2=26 kJ·mol-1
H2O (g)=H2O(l) ΔH3=-44 kJ·mol-1
则反应CaSO4·![]() H2O(s)=CaSO4(s)+
H2O(s)=CaSO4(s)+ ![]() H2O(g)的ΔH4=_________kJ·mol-1。
H2O(g)的ΔH4=_________kJ·mol-1。
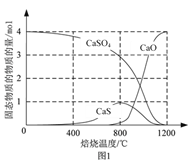
⑵用合适的还原剂可以将CaSO4还原,所得SO2可用于工业生产硫酸。
①以CO作还原剂,改变反应温度可得到不同的产物。不同温度下反应后所得固体成分的物质的量如图1所示。在低于800 ℃时主要还原产物为___________;高于800 ℃时主要发生的反应的化学方程式为___________。
②以高硫煤为还原剂焙烧2.5 小时,不同条件对硫酸钙转化率的影响如下图2所示。CaCl2的作用是___________;当温度高于1200 ℃时,无论有无CaCl2,CaSO4的转化率趋于相同,其原因是___________。

③以C作还原剂,向密闭容器中加入相同质量的几组不同C/S值(炭粉与CaSO4的物质的量之比)的混合物在1100 ℃加热,结果如上图3所示。当C/S值为0.5时,反应产物为CaO、SO2和CO2;当C/S值大于0.7时,反应所得气体中SO2的体积分数不升反降,其主要原因可能是___________。
⑶利用反应CaSO4(s)+(NH4)2CO3(aq)![]() CaCO3(s)+(NH4)2SO4(aq)可以将磷石膏转化为硫酸铵。若反应达到平衡后溶液中c(SO42-)=2.0 mol·L-1,此时溶液中c(CO32-)=___________。(已知Ksp(CaCO3)=2.8×10-9,Ksp(CaSO4)=3.2×10-6)
CaCO3(s)+(NH4)2SO4(aq)可以将磷石膏转化为硫酸铵。若反应达到平衡后溶液中c(SO42-)=2.0 mol·L-1,此时溶液中c(CO32-)=___________。(已知Ksp(CaCO3)=2.8×10-9,Ksp(CaSO4)=3.2×10-6)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下例说法中正确的是( )
A 在分子中,两个成键的原子间的距离叫做键长
B.含有极性键的分子一定是极性分子
C.键能越大,表示该分子越容易分解
D.H-Cl的键能为431.8KJ/mol-1,H-I的键能为298.7KJ/mol-1,这可以说明HCl分子比HI分子稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某链烃3.6g和Cl2发生取代反应,控制反应条件使其仅生成一氯代物,将反应生成的气体(一氯代物为液体)用NaOH溶液吸收恰好和0.1molL-1NaOH溶液500mL完全反应,试解答下列问题:
(1)求该烃的相对分子质量_______________;
(2)若该烃既不能使酸性KMnO4溶液褪色,又不能使溴水褪色,试求该烃的分子式____________。
(3)若该烃的一氯代物只有一种,试确定该烃的结构简式(要求写出计算过程)_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香化合物A、B互为同分异构体,B的结构简式是![]() 。A经①、②两步反应得C、D和E。B经①、②两步反应得E、F和H。上述反应过程、产物性质及相互关系如图所示。E的分子式为C7H6O3
。A经①、②两步反应得C、D和E。B经①、②两步反应得E、F和H。上述反应过程、产物性质及相互关系如图所示。E的分子式为C7H6O3

提示:![]()
(1)写出E的结构简式______________。
(2)A有2种可能的结构,写出相应的结构简式_______________。
(3)在B、C、D、F、G、I化合物中,互为同系物的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是一种军用催泪弹的主要有效成分。经分析A的相对分子质最为161,且分子中只含有一个甲基。化合物A~F的转化关系如下图所示,其中足量的新制Cu(OH)2悬浊液与1molC反应可生成1molCu2O和lmolD, B1和B2均为较稳定的化合物且互为同分异构体。
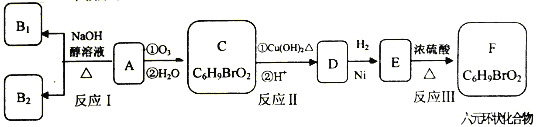
已知:①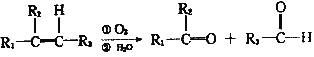
② 一个碳原子上连有两个碳碳双键的结构不稳定。
请完成下列问题:
(l)B1的相对分子质量是_______;
(2)C中的官能团有醛基、_______;
(3)写出A 与热的烧碱水溶液反应的化学方程式:______________;
(4)写出反应Ⅲ的化学方程式:__________________;
(5)写出符合下列条件的E的所有同分异构体_______。
① 含有兰个甲基;② 自身能发生酯化反应;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化两面针碱(H)具有抑制肿瘤细胞增殖和诱杀作用,被认定为潜在的抗肿瘤药物。其合成路线如下:
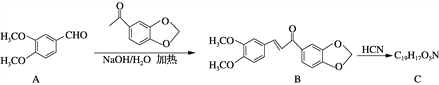
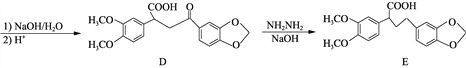
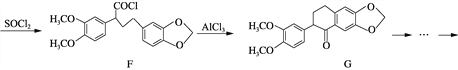
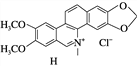
(1) 化合物B中含氧官能团的名称为________和________。
(2) 化合物C的结构简式为______________;
由E→F的反应类型为______________。
(3) 写出同时满足下列条件的A的一种同分异构体的结构简式________。
①能与FeCl3溶液发生显色反应,②既能发生银镜反应又能发生水解反应;③分子中只含4种不同化学环境的氢。
(4) 请以C6H5CH2CH2CH2OH为原料制备![]() ,写出制备的合成路线流程图__________ (无机试剂任用,合成路线流程图示例见本题题干)。
,写出制备的合成路线流程图__________ (无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com