

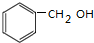
 ,乙酸和苯甲醇反应生成乙酸苯甲酯,据此分析解答.
,乙酸和苯甲醇反应生成乙酸苯甲酯,据此分析解答. ,乙酸和苯甲醇反应生成乙酸苯甲酯,
,乙酸和苯甲醇反应生成乙酸苯甲酯,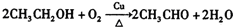 ,故答案为:
,故答案为: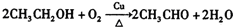 ;
; ,其官能团名称是醇羟基,故答案为:醇羟基;
,其官能团名称是醇羟基,故答案为:醇羟基;

科目:高中化学 来源: 题型:
| 催化剂 |
| 加热、加压 |

| 物质 | CH3OH | CH3OCH3 | H2O |
| c/mol?L-1 | 0.44 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴定前酸式滴定管尖嘴部分有气泡,滴定终止时气泡消失 |
| B、锥形瓶用蒸馏水洗净后,未经干燥即进行滴定 |
| C、滴定过程中,锥形瓶中有溶液溅出 |
| D、酸式滴定管未用标准盐酸润洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2个 | B、3个 | C、4个 | D、5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 Cu、Zn、稀H2SO4形成如图甲乙装置.
Cu、Zn、稀H2SO4形成如图甲乙装置.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、υ(A)=0.2mol(L?s) |
| B、υ(B)=0.45 mol(L?s) |
| C、υ(C)=0.40 mol(L?min) |
| D、υ(D)=0.6 mol(L?min) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com