
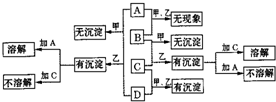
 A、B、C、D分别代表硝酸银、偏铝酸钠、稀盐酸、浓氨水四种无色溶液中的一种.甲、乙两同学按不同体积比进行了两两混合,实验现象如下:
A、B、C、D分别代表硝酸银、偏铝酸钠、稀盐酸、浓氨水四种无色溶液中的一种.甲、乙两同学按不同体积比进行了两两混合,实验现象如下: ,
, .
.

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
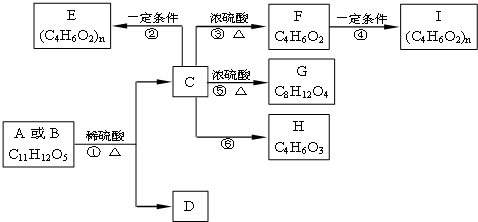
 ,现有A、B、C、D、E、F、G、H八种有机物,存在如下图所示的转化关系:
,现有A、B、C、D、E、F、G、H八种有机物,存在如下图所示的转化关系:
| 序号 | ① | ② | ③ | ④ | ⑤ |
| 无机反应物 | NaOH溶液 | 盐酸 | 新制Cu(OH)2 | 稀硫酸 | H2O |
| 反应条件 | 加热 | - | 加热 | 加热 | 催化剂 HgSO4 |
| 催化剂 |
| 催化剂 |




查看答案和解析>>
科目:高中化学 来源: 题型:
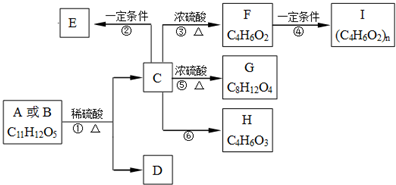
 (其中R为饱和烃基),A在一定条件下有如图所示的转化关系.已知E的蒸气密度是相同条件下H2密度的74倍,分子组成符合CaHbO2.
(其中R为饱和烃基),A在一定条件下有如图所示的转化关系.已知E的蒸气密度是相同条件下H2密度的74倍,分子组成符合CaHbO2.










查看答案和解析>>
科目:高中化学 来源: 题型:
二甲基苯中苯环上的一溴代物有 种同分异构体,分别对应三种二甲苯,其熔点见表格:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
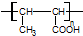
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com