
【题目】有机玻璃是一种重要的塑料,有机玻璃的单体A(C5H8O2)不溶于水,并可以发生以下变化:

请回答:
(1)B分子中含有的官能团是________、________。
(2)由B转化为C的反应属于________(选填序号)。
①氧化反应 ②还原反应 ③加成反应 ④取代反应
(3)C的一氯代物D有两种,C的结构简式是________。
(4)由A生成B的化学方程式是___________________________________。
(5)有机玻璃的结构简式是______________________________________。
【答案】 碳碳双键 羧基 ②③ CH3CH(CH3)COOH CH2=C(CH3)COOCH3+H2O![]() CH2=C(CH3)COOH+CH3OH
CH2=C(CH3)COOH+CH3OH 
【解析】根据框图中信息A能发生加聚反应,说明其中含有碳碳双键;同时A又能水解生成甲醇,说明A属于酯,B属于羧酸,因此,B中必然含有羧基﹣COOH;又知A水解过程中破坏的只是酯基,而碳碳双键保留了下来,B中应还含有C=C双键,B能与氢气发生加成反应也说明了B含有C=C双键,根据A的分子中有5个碳原子,而它水解又生成了甲醇和B,因此B中有4个碳原子,B转化成C的过程中没有碳原子的变化,即C中也只有4个碳原子,C的一氯代物D有两种,得出C的结构简式为CH3CH(CH3)COOH,故B为CH2=C(CH3)COOH,A为CH2=C(CH3)COOCH3,A加聚反应生成有机玻璃,机玻璃的结构简式是: ,
,
(1)B为CH2=C(CH3)COOH,含有碳碳双键、羧基,
(2)CH2=C(CH3)COOH与氢气发生加成反应生成CH3CH(CH3)COOH,该反应也属于还原反应,
(3)由上述分析可知,C为CH3CH(CH3)COOH,
(4)CH2=C(CH3)COOCH3在浓硫酸、加热条件下水解生成甲醇与CH2=C(CH3)COOH,反应方程式为:
CH2=C(CH3)COOCH3+H2O![]() CH2=C(CH3)COOH+CH3OH,
CH2=C(CH3)COOH+CH3OH,
(5)CH2=C(CH3)COOCH3发生加聚反应生成有机玻璃,机玻璃的结构简式是: ,
,


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】为确定盐酸、碳酸、硅酸的酸性强弱,设计了如图所示的装置,一次实验即可达到目的(不必选其他酸性物质)。(提示:检验酸的酸性强弱可用强酸制取弱酸)

(1)锥形瓶中装某可溶性正盐,分液漏斗中所盛试剂应为________。
(2)装置B中所盛试剂是________________________________________,其作用是_____________。
(3)装置C中所盛试剂是___________________________________________,
C中反应的离子方程式是_________________________________________________。
(4)由此得到的结论是酸性:________>________>________。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写出方程式。
(1)CH3CH==CHCHO与足量的氢气一定条件下反应:____________________________。
(2)CH2ClCH2CH2OH在浓硫酸催化下加热:_____________________________________。
(3)苯酚中加足量浓溴水:___________________________________。
(4) nHOCH2CH2COOH→ ________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是______(填字母序号)。
a.Fe b.FeO c.Fe3O4 d.Fe2O3
(2)硫酸渣的主要化学成分为:SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
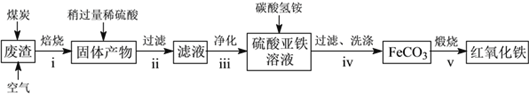
回答下列问题:
①在步骤i中产生的有毒气体可能有__________________。
②在步骤iii操作中,要除去的离子之一为Al3+。若常温时Ksp[Al(OH)3]=1.0×10-32,此时理论上将Al3+沉淀完全,则溶液的pH为____________。
③步骤iv中,生成FeCO3的离子方程式是_________________。
(3)氯化铁溶液称为化学试剂中的“多面手”,向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生新的沉淀,写出该沉淀的化学式_________________。请用平衡移动的原理,结合必要的离子方程式,对此现象作出解释:___________________。
(4)①古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应ii的离子方程式是________________。
②如今基于普鲁士蓝合成原理可检测食品中CN-,方案如下:
![]()
若试纸变蓝则证明食品中含有CN-,请解释检测时试纸中FeSO4的作用:
_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】升高温度能加快反应速率的主要原因是 ( )
A. 活化分子能量明显增加 B. 降低活化分子能量 C. 增加活化分子百分数 D. 降低反应所需能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积0.1mol·L-1的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示则

A. M点所示溶液的导电能力强于Q点
B. N点所示溶液中c(CH3COO-)>c(Na+)
C. M点和N点所示溶液中水的电离程度相同
D. Q点消耗NaOH溶液的体积等于醋酸溶液的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水是用氯气杀菌消毒的,不法商贩用自来水冒充纯净水销售,为辨别纯净水真伪,可用下列哪种试剂鉴别( )
A.酚酞试液
B.氯化铁溶液
C.硝酸银溶液
D.氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁的单质及其化合物用途非常广泛。
(1)镁热还原法可制备铷、钛等金属,已知下列物理常数:
Mg | Rb | RbCl | MgCl2 | |
熔点/℃ | 648 | 38.89 | 718 | 714 |
沸点/℃ | 1107 | 688 | 1390 | 1412 |
在750℃时可实现用镁还原RbCl制Rb,该反应能够发生的原因是_________________________________(用文字和化学方程式说明)。
(2)无机抗菌剂Mg2ClO(OH)3·H2O(碱式次氯酸镁)可由MgCl2、NaOH及Cl2反应制得,该反应的化学方程式为______________________________________。
(3)CaC2冶镁的原理为CaC2(s)+MgO(s)![]() CaO(s)+Mg(g)+2C(s) △H,反应达到平衡时Mg的产率随温度的变化如图所示。
CaO(s)+Mg(g)+2C(s) △H,反应达到平衡时Mg的产率随温度的变化如图所示。

①△H__________(填“>"或“<”,下同)0。
②已知A、B中固体总质量相等,则![]() :A__________B。
:A__________B。
(4)Mg(OH)2浆液可脱除烟气中的SO2,其脱硫效率、pH及时间的关系如图所示。

Mg(OH)2浆液脱除SO2的过程中包含的主要反应如下:
Ⅰ.Mg(OH)2+SO2=MgSO3+H2O
Ⅱ.MgSO3+SO2+H2O=Mg(HSO3)2
Ⅲ.Mg(HSO3)2+Mg(OH)2=2MgSO3+2H2O
Ⅳ.2MgSO3+O2=2MgSO4
已知:20℃时,H2SO3的电离平衡常数K1=1.54×10-2、K2=1.02×10-7;25℃时,Ksp[Mg(OH)2]=1.2×10-11,MgSO3,的溶解度为0.646g。
①脱硫过程中使浆液pH减小最显著的反应是__________(填“Ⅰ”“Ⅱ”“Ⅲ”或“Ⅳ”)。
②约900s之后,脱硫效率明显降低,其原因是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com