
| A. | 硅是良好的半导体材料 | |
| B. | 二氧化硅能与石灰石反应:SiO2+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑ | |
| C. | 可以用焦炭还原二氧化硅生产硅:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑ | |
| D. | 水泥的主要成分是 Na2SiO3、CaSiO3 和 SiO2 |
分析 A.Si处于金属和非金属元素之间,具有金属和非金属的性质,其单质属于半导体材料;
B、二氧化硅与碳酸盐反应生成硅酸盐和二氧化碳;
C、焦炭与二氧化硅在高温条件下反应生成粗硅和一氧化碳;
D、水泥的主要成分为:硅酸三钙、硅酸二钙、铝酸三钙.
解答 解:A.Si处于金属和非金属元素之间,具有金属和非金属的性质,其单质属于半导体材料,可以作硅芯片和硅太阳能电池,故A正确;
B、二氧化硅与碳酸盐反应生成硅酸盐和二氧化碳,所以二氧化硅能与石灰石反应:SiO2+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑,故B正确;
C、焦炭与二氧化硅在高温条件下反应生成粗硅和一氧化碳,所以反应方程式为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,故C正确;
D、水泥的主要成分为:硅酸三钙、硅酸二钙、铝酸三钙,故D错误;
故选D.
点评 本题考查硅及其化合物的性质,侧重考查基本概念、基本理论等知识点,题目难度不大,注意相关知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| B. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 | |
| C. | 高温和日常用的消毒剂均可使禽流感病毒变性 | |
| D. | 误食重金属盐引起人体中毒,可饮用大量的食盐水解毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
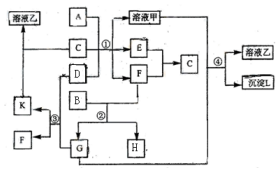 如图表示常见的单质及其化合物之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略).
如图表示常见的单质及其化合物之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ①②③④ | C. | ①③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应Ⅰ中HCl是氧化剂 | B. | 反应Ⅱ中Cl2被氧化,发生氧化反应 | ||
| C. | 还原性:CoCl2>HCl>I2 | D. | 氧化性:Co2O3>Cl2>HIO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 化学反应 | 离子方程式 | 评价 |
| A | 碳酸钙与盐酸 | CO32-+2H+=H2O+CO2↑ | 错误,碳酸钙是弱电解质,不应写成离子形式 |
| B | 向次氯酸钙溶液通入过量CO2 | Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | 正确 |
| C | 石灰水中滴加少量NaHCO3溶液 | Ca2++HCO3-+OH-=CaCO3↓+H2O | 错误,不满足Ca(OH)2的配比 |
| D | 过量铁屑溶于稀硝酸 | 3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O | 正确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由水电离的c(H+):①=②>③=④ | |
| B. | 将②、③两种溶液混合后,若pH=7,则消耗溶液的体积:②=③ | |
| C. | 等体积的①、②两种溶液分别与足量铝粉反应,生成H2的量相等 | |
| D. | 向等体积四种溶液中分别加水至体积为原来的100倍后,溶液的pH:③>④>②>① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com