
【题目】某有机物X( )是我国具有自主知识产权的国家一类新药的有效成分,下列关于X的说法错误的是
)是我国具有自主知识产权的国家一类新药的有效成分,下列关于X的说法错误的是
A.1 mol X与足量H2发生加成反应消耗3 mol H2B.与酸和与碱反应的类型相同
C.分子中所有碳原子在同一平面内D.一氯取代物只有6种
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
【题目】如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是( )
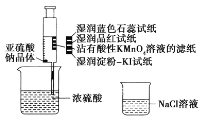
A. 湿润淀粉-KI试纸未变蓝说明SO2的氧化性弱于I2
B. 蓝色石蕊试纸先变红后褪色
C. NaCl溶液可用于除去实验中多余的SO2
D. 品红试纸、沾有酸性KMnO4溶液的滤纸均褪色,证明SO2具有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.100 mol·L-1 AgNO3滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所示。下列有关描述错误的是
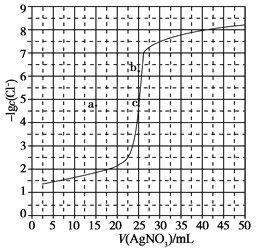
A. 根据曲线数据计算可知Ksp(AgCl)的数量级为10-10
B. 曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=Ksp(AgCl)
C. 相同实验条件下,若改为0.0400 mol·L-1 Cl-,反应终点c移到a
D. 相同实验条件下,若改为0.0500 mol·L-1 Br-,反应终点c向b方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年政府工作报告提出要持续开展大气污染的治理攻坚。下列与大气污染防治无关的是
A.海水晒盐
B.汽车尾气净化减排
C.工业尾气回收处理
D.利用清洁能源替代化石燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,C和H2O(g)在密闭容器里发生下列反应:
①C(s)+H2O(g)![]() CO(g)+H2(g), ②CO(g)+H2O(g)
CO(g)+H2(g), ②CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
当反应达到平衡时,c(H2)=1.9 mol·L-1,c(CO)=0.1 mol·L-1。则下列叙述正确的有
A. CO在平衡时转化率为10%
B. 平衡浓度c(CO2)=c(H2)
C. 平衡时气体平均相对分子质量约为23.3
D. 其他条件不变时,缩小体积,H2O(g)的转化率随之降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释实验事实的方程式不正确的是
A.铁粉与水蒸气反应产生一种可燃气体:3Fe + 4H2O(g)![]() Fe3O4 + 4H2
Fe3O4 + 4H2
B.NO2能溶于水且溶液显酸性:NO2 + H2O= 2H+ + NO3
C.氯气能使湿润的有色布条褪色:Cl2+H2O![]() H+ + Cl + HClO
H+ + Cl + HClO
D.Na2O2能与水反应产生使带火星的木条复燃的气体:2Na2O2+2H2O== 4Na+ + 4OH + O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某高中科研小组模拟工业尿素法生产肼(N2H4),具体方法:先将尿素、次氯酸钠和氢氧化钠溶液混合,然后在催化剂存在的条件下反应制得肼,利用氮气吹出混合物中的肼,并用硫酸吸收制备硫酸肼。具体实验原理图如下:
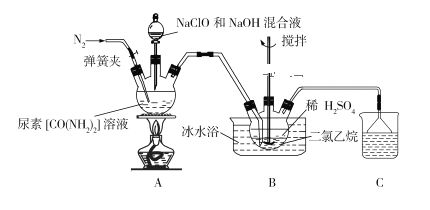
已知:①肼极易溶于水,长期暴露在空气中或短时间受高温作用会爆炸分解。
②硫酸肼(N2H4·H2SO4)是类似于NH4HSO4的盐类,白色固体,微溶于冷水,易溶于热水,不溶于乙醇和二氯乙烷等有机溶剂。
③密度:ρ硫酸肼>ρ二氯乙烷>ρ稀硫酸
(1)盛装尿素溶液的装置名称为_____________________;硫酸肼的水溶液中含有多种阳离子,其中阳离子N2H5+的电子式为________________________。
(2)反应前应先通入一段时间氮气,其目的为________________________________。
(3)装置A中发生反应制备肼的离子方程式为_______________________________。
(4)装置B中二氯乙烷的作用为__________________________________________;使用冰水浴的作用__________________________________________________。
(5)装置B反应完全后需经过过滤、洗涤、干燥等操作得到硫酸肼,洗涤过程中最好选择下列那种洗涤剂________________(填字母)。
A.冷水 B.热水 C.无水乙醇 D.饱和食盐水
(6)若实验中所用的NaClO和NaOH混合液中两溶质的浓度均为0.1mol·L1,则此溶液中离子浓度的大小顺序为______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧氟沙星是常用抗菌药,其结构简式如图所示,下列对氧氟沙星叙述错误的是
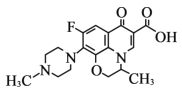
A.能发生加成、取代反应B.能发生酯化反应
C.分子内共有19个氢原子D.分子内共平面的碳原子多于6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2可用于防腐剂、消毒剂,也是一种重要的冷冻介质。实验室可用如图所示装置制备SO2,并用纯净SO2进行相关实验。
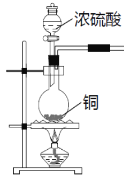
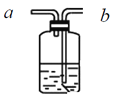
(1)上述方法制备的SO2中,往往因伴有硫酸小液滴而呈白雾状。除去白雾可在制备装置后连接下图所示装置,该装置中的试剂是__________,气体从_______口(填“a”或“b”)进。
(2)检验SO2常用的试剂是__________________,利用了SO2的_________性。
(3)将SO2通入0.1mol/L Ba(NO3)2溶液中,得到白色沉淀,该沉淀的化学式为___________。
分别用煮沸和未煮沸过的蒸馏水配制Ba(NO3)2和BaCl2溶液,进行如下实验:
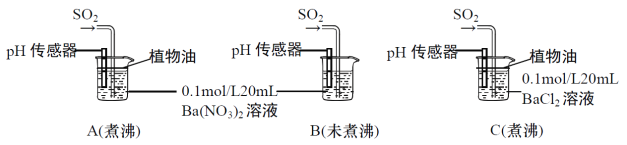
(4)实验A、C中,煮沸蒸馏水及使用植物油的目的是_________________________________。
(5)实验C中,没有观察到白色沉淀,但pH传感器显示溶液呈酸性,原因是__________________。(用方程式表示)
(6)实验B中出现白色沉淀比实验A快很多。由此得出的结论是___________________________。若实验A、B中通入足量的SO2后,溶液pH:A_________B(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com